
【题目】为体现节能减排的理念,中国研制出了新型固态氧化物燃料电池(SOFC),该电池的工作原理如图所示。下列说法正确的是( )
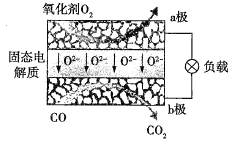
A.可以选用NaOH固体作固态电解质
B.正极的电极反应式为O2+4e-+2H2O=4OH-
C.电子从b极经导线流向a极
D.若反应中转移1 mol电子,则生成22.4 L(标准状况下)CO2
【答案】C
【解析】
该燃料电池中,CO是燃料,所以CO失电子发生氧化反应,则CO所在的b电极为负极,通入氧气的a电极是正极,正极上氧气得电子发生还原反应,电子从负极沿外电路流向正极,据此分析解答。
A.因为NaOH与CO2会发生反应,所以不可以选用NaOH固体作固态电解质,A错误;
B.通入氧气的a电极是正极,正极上氧气得电子发生还原反应,电极反应式为O2+4e-=2O2-,B错误;
C.外电路中,电子从负极b极经导线流向正极a极,C正确;
D.CO所在的b电极为负极,电极反应式为CO-2e-+O2-=CO2,所以反应中转移1 mol电子,则生成0.5 mol CO2,温度压强不知不能计算气体体积,D错误;
故合理选项是C。


科目:高中化学 来源: 题型:
【题目】I.在①苯 ②苯酚 ③甲苯 ④氯乙烷 ⑤乙烯 ⑥乙醇中,(填编号)
<1>能和金属钠反应放出H2的有______ <2>能与NaOH溶液反应的有______
<3>常温下能与溴水反应的有_________ <4>能使酸性KMnO4溶液褪色的烃有_______
II.已知某有机物的结构简式为: ![]()
①该有机物中所含官能团的名称是________________________。
②该有机物发生加聚反应后,所得产物的结构简式为__________。
③写出该有机物发生消去反应的化学方程式(注明反应条件):_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 25℃下时,NH3·H2O kb=1.77×10-5;H2CO3 ka1=4.30×10-7、ka2=5.61×10-11。 25℃时有关NH4HCO3溶液的说法中正确的是
A. 呈弱酸性
B. c(OH-)+c(NH3·H2O)=c(H+)+c(H2CO3)
C. 滴入NaOH 溶液发生反应:NH4++OH-=NH3·H2O和HCO3-+OH-=H2O+CO32-
D. 滴入NaOH溶液,则![]() 增大
增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属锂及其化合物用途广泛。其在“氮的固定”中转化过程如图所示:
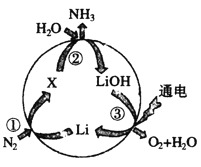
(1)图中X的化学式为__________。
(2)图中所示物质既含共价键、又含离子键的是_______(填化学式),属于电解质的有______种。
(3)③中阳极电极反应式为____________________。
(4)图中所示过程总转化关系式为_______________。
(5)Li也可用于空气中CO2的固定,其工作原理为:4Li+3CO2![]() 2Li2CO3+C。电池的电解质称为电池的“血液”,该电池的电解质应为_______________(填化学式)。正极电极反应式为_________________________________。反应中当有3mol氧化剂被还原,通过交换膜的Li+为_________mol。
2Li2CO3+C。电池的电解质称为电池的“血液”,该电池的电解质应为_______________(填化学式)。正极电极反应式为_________________________________。反应中当有3mol氧化剂被还原,通过交换膜的Li+为_________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于苯乙烯(![]() )有下列叙述:① 能使酸性KMnO4溶液褪色;② 能使溴的四氯化碳溶液褪色;③ 可溶于水;④ 可溶于苯中;⑤ 能与浓硝酸发生取代反应;⑥ 所有的原子可能共平面。其中正确的是( )
)有下列叙述:① 能使酸性KMnO4溶液褪色;② 能使溴的四氯化碳溶液褪色;③ 可溶于水;④ 可溶于苯中;⑤ 能与浓硝酸发生取代反应;⑥ 所有的原子可能共平面。其中正确的是( )
A. ①②③④⑤ B. ①②⑤⑥ C. ①②④⑤⑥ D. 全部正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乳酸亚铁晶体{[CH3CH(OH)COO]2Fe·3H2O}(相对分子质量:288)可由乳酸与FeCO3反应制得,它易溶于水,几乎不溶于乙醇,受热易分解,是一种很好的补铁剂。
I.制备碳酸亚铁:装置如图所示。
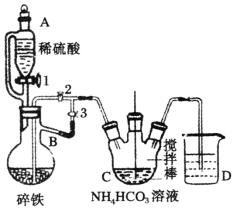
(1)仪器B的名称是_________________________。
(2)实验操作如下:关闭活塞2,打开活塞1、3,加入适量稀硫酸反应一段时间,其目的是:__________,然后关闭活塞1,接下来的操作是:______。C中发生反应的离子方程式为_____________。
Ⅱ.制备乳酸亚铁:
向纯净的FeCO3固体加入足量乳酸溶液,在75℃下搅拌使之充分反应。
(3)该反应化学方程式为______。为防止乳酸亚铁变质,在上述体系中还应加入____。反应结束后,从所得溶液中获得乳酸亚铁晶体的方法是:_________,冷却结晶,过滤,_________,干燥。
Ⅲ.乳酸亚铁晶体纯度的测量:
(4)用K2Cr2O7滴定法测定样品中Fe2+的含量计算样品纯度,称取6.00g样品配制成250.00mL溶液.取25.00mL用0.0167mol·L-1的K2Cr2O7标准溶液滴定至终点,消耗标准液20.00mL。则产品中乳酸亚铁晶体的纯度为___(以质量分数表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器,一定条件下进行反应:mA(g)+nB(g)pC(g)+qD(g)。若增大压强或升高温度,重新达到平衡,变化过程均如图所示,则对该反应叙述正确的是( )
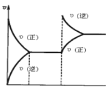
A.m+n<p+qB.逆反应是放热反应
C.m+n>p+qD.正反应是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol·L-1的三种酸(HA、HB和HD)溶液,滴定的曲线如图所示,下列判断错误的是( )
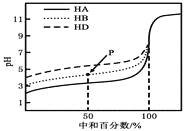
A. 三种酸的电离常数关系:KHA>KHB>KHD
B. 滴定至P点时,溶液中:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-)
C. pH=7时,三种溶液中:c(A-)=c(B-)=c(D-)
D. 当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH-)-c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,对应的操作、现象以及所得出的结论都正确的是( )
选项 | 实验 | 现象 | 结论 |
A. | 把铝箔插入浓硝酸中 | 有大量红棕色气体产生 | 浓硝酸具有强氧化性 |
B. |
| 品红褪色 |
|
C. | 淀粉在酸催化水解后的溶液加入新制 | 无砖红色沉淀 | 淀粉水解产物不含葡萄糖 |
D. | 将充满 | 红棕色变深 | 反应 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com