


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

 得到碘酸钾晶体,你建议的方法是
得到碘酸钾晶体,你建议的方法是| 温度/℃ | 0 | 10 | 20 | 40 | 60 | 80 |
| KIO3g/100g水 | 4.60 | 6.27 | 8.08 | 12.6 | 18.3 | 24.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||




查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
阳离子交换膜能在直流电场的作用下选择性地透过电解液中的阳离子使向阴极迁移,阴离子交换膜则能在直流电场的作用下选择性地透过电解液中的阴离子使向阳极迁移。同时在电解槽(称为“电渗析器”)中使用合适型号的这两种膜(简称“阳膜”和“阴膜”),可以在直流电场的作用下进行海水的电渗析脱盐而使海水淡化。
海水中主要离子的含量平均值如下:
Cl-18 980 mg·L-1,Na+:10 560 mg·L-1,![]() :2 560 mg·L-1,Mg2+:1 272 mg·L-1,Ca2+:400 mg·L-1,K+:380 mg·L-1,HCO3-:142 mg·L-1
:2 560 mg·L-1,Mg2+:1 272 mg·L-1,Ca2+:400 mg·L-1,K+:380 mg·L-1,HCO3-:142 mg·L-1
海水在电渗析器中部分变成淡水的原理,示意图如图2-21所示电渗析器中由许多对阳、阴膜围成的许多“隔室”的宽度都很窄。脱盐时,各隔室相间流动着“淡水”和“浓水”;在流动着“极水”的以石墨为电极材料的两极发生电解反应。根据需要,可将几台电渗析器串联使用。图中标写的离子符号,提供思考其在电场中的迁移方向。

图2-21
回答下列问题:
(1)分别写出海水在电渗析器中脱盐时所得主要阳极产物和主要阴极产物的化学式。用以石棉布为隔膜的一般的惰性阳极电解槽来电解海水,能用以生产H2吗?为什么?
(2)致力于发展电渗析法、反渗透法等海水淡化新技术的直接社会效益是什么?
(3)已成功地联合应用海水淡化新技术和一般的离子交换树脂净水法,由海水制得纯水。又知海洋水能源(海洋水能发电)有其巨大的开发前景。你认为应怎样综合开发海洋能源,促成人类进入氢能时代?
查看答案和解析>>
科目:高中化学 来源:2012-2013学年山东省济宁市高三4月联考理综化学试卷(解析版) 题型:填空题
某科研小组以难溶性钾长石(K2O•Al2O3•6SiO2)为原料,提取Al2O3、K2CO3等物质,工艺流程如下:
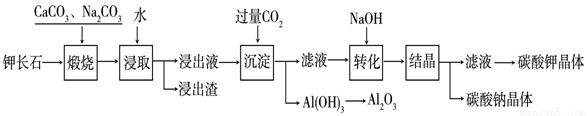
(1)煅烧过程中钾长石中的钾元素和铝元素在Na2CO3作用下转化为可溶性的NaAlO2和KAlO2,写出Al2O3转化为NaAlO2的化学方程式是: 。
(2)已知NaAlO2和KAlO2易发生如下水解反应:AlO2—+ 2H2O 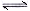 Al(OH)3
+ OH— ,“浸取”时应保持溶液呈
性(填“酸”或“碱”)。
Al(OH)3
+ OH— ,“浸取”时应保持溶液呈
性(填“酸”或“碱”)。
(3)“转化”时加入NaOH的主要作用是 (用离子方程式表示)。
(4)上述工艺中可以循环利用的主要物质是 、 和水。
(5)以Al2O3为原料,以石墨为电极,通过电解法可制得金属铝。电解池中接电源负极的一极的电极反应式是 。长时间电解后,需要更换新的石墨电极的是 极(填“阴”或“阳”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com