
【题目】碳酸镧[La2(CO3)3]可用于治疗高磷酸盐血症。某化学小组用如图装置模拟制备碳酸镧,反应为2LaCl3+6NH4HCO3=La2(CO3)3↓+6NH4Cl+3CO2↑+3H2O下列说法正确的是
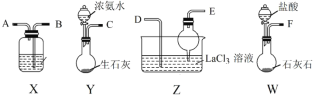
A.从左向右接口的连接顺序:F→B,A→D,E←C
B.装置X中盛放的试剂为饱和Na2CO3溶液
C.实验开始时应先打开W中分液漏斗的旋转活塞
D.装置Z中用干燥管的主要目的是增大接触面积,加快气体溶解
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】卤代烃是重要的工业原料,同时对环境造成严重影响,如破坏臭氧层等,请回答下列问题:
Ⅰ.氟利昂-12,即二氟二氯甲烷,分子式为![]() ,氟利昂-11,即一氟三氯甲烷,分子式为
,氟利昂-11,即一氟三氯甲烷,分子式为![]() 。氟利昂是破坏臭氧层的元凶,也是地球变暖的罪魁祸首,它所产生的温室效应是二氧化碳的数千倍。禁止使用氟利昂对保护地球环境具有极为重要的意义。破坏臭氧层的物质有制冷剂
。氟利昂是破坏臭氧层的元凶,也是地球变暖的罪魁祸首,它所产生的温室效应是二氧化碳的数千倍。禁止使用氟利昂对保护地球环境具有极为重要的意义。破坏臭氧层的物质有制冷剂![]() 等氟氯烃其破坏机理为
等氟氯烃其破坏机理为![]() 。
。
(1)活性氯(![]() )的作用是__________;
)的作用是__________;
(2)下列关于氟利昂![]() 、氟利昂
、氟利昂![]() 的推测不正确的有______________;
的推测不正确的有______________;
A 两种氟利昂在![]() 醇溶液中均可发生消去反应
醇溶液中均可发生消去反应
B 两种氟利昂均不存在同分异构体
C 直接用![]() 溶液均可检验两种氟利昂中的氯元素
溶液均可检验两种氟利昂中的氯元素
Ⅱ.已知二氯烯丹是一种除草剂,其合成路线如下:
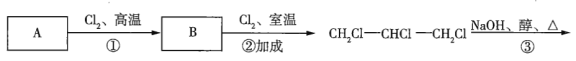
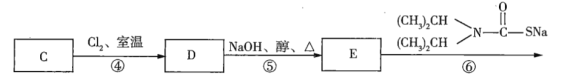
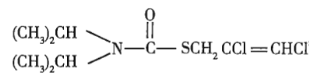 (二氯烯丹)
(二氯烯丹)
已知:D在反应⑤中所生成的E的结构只有一种。
(1)写出下列反应类型:反应①是___________,反应③是________,反应⑥是__________;
(2)写出下列物质的结构简式:A______,C______;
(3)写出反应③的化学反应方程式___________;
(4)写出有机物![]() 所有同分异构体的结构简式:________。
所有同分异构体的结构简式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】连二次硝酸(H2N2O2)是二元酸,可用于制N2O气体。
(1)连二次硝酸中氮元素的化合价为___。
(2)常温下,用0.01mol·L-1NaOH溶液滴定10mL0.01mol·L-1H2N2O2溶液,测得溶液pH与NaOH溶液体积的关系如图所示。
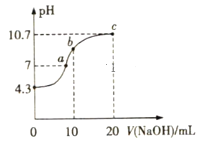
写出H2N2O2在水溶液中电离的主要方程式:___。
②c点时溶液中下列离子Na+、OH-、N2O22-、HN2O2-,浓度由大到小的顺序为___。
③b点时溶液中的溶质为___。
④a点时溶液中c(Na+)___c(HN2O2-)+c(N2O22-)(填“>”“<”或“=”)。
(3)硝酸银溶液和连二次硝酸钠溶液混合,可得到黄色的连二次硝酸银沉淀,向该体系中滴加硫酸钠溶液,白色沉淀和黄色沉淀共存时,该体系中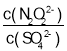 =___[已知Ksp(Ag2N2O2)=4.2×10-9,Ksp(Ag2SO4)=1.4×10-5].
=___[已知Ksp(Ag2N2O2)=4.2×10-9,Ksp(Ag2SO4)=1.4×10-5].
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 的两种一元酸
的两种一元酸![]() 和
和![]() ,体积均为
,体积均为![]() ,稀释过程中
,稀释过程中![]() 与溶液体积的关系如图所示。分别滴加
与溶液体积的关系如图所示。分别滴加![]() 溶液(
溶液(![]() )至
)至![]() ,消耗
,消耗![]() 溶液的体积为
溶液的体积为![]() 、
、![]() ,则( )
,则( )
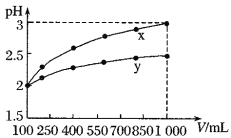
A.![]() 为弱酸,
为弱酸,![]()
B.![]() 为强酸,
为强酸,![]()
C.![]() 为弱酸,
为弱酸,![]()
D.![]() 为强酸,
为强酸,![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝在酸性或碱性溶液中均可与NO3—发生氧化还原反应,转化关系如下图所示:
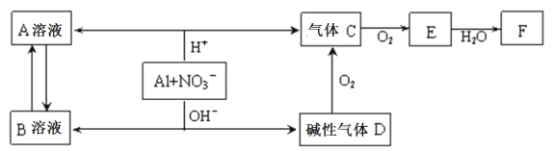
下列说法错误的是
A.B溶液含[Al(OH)4]—
B.A溶液和B溶液混合无明显现象
C.D与F反应生成盐
D.E排入大气中会造成污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于自然界中氮循环(如图)的说法不正确的是:

A. 氮元素均被氧化
B. 工业合成氨属于人工固氮
C. 含氮无机物和含氮有机物可相互转化
D. 碳、氢、氧三种元素也参与了氮循环
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
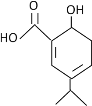
A.如图有机物核磁共振氢谱中出现8组峰
B.如图有机物分子式为C10H12O3
C.分子式为C9H12的芳香烃共有9种
D.蓝烷![]() 的一氯取代物共有6种(不考虑立体异构)
的一氯取代物共有6种(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖颁给了日本吉野彰等三人,以表彰他们对锂离子电池研发的卓越贡献。
(1)工业中利用锂辉石(主要成分为LiAlSi2O6,还含有FeO、CaO、MgO等)制备钴酸锂(LiCoO2)的流程如图:
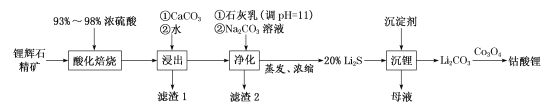
回答下列问题:
①锂辉石的主要成分为LiAlSi2O6,其氧化物的形式为___。
②为提高“酸化焙烧”效率,常采取的措施是___。
③向“浸出液”中加入CaCO3,其目的是除去“酸化焙烧”中过量的硫酸,控制pH使Fe3+、A13+完全沉淀,则pH至少为___。(已知:,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Al(OH)3]=1.0×10-33,完全沉淀后离子浓度低于1×l0-5)mol/L)。
④“滤渣2”的主要化学成分为___。
⑤“沉锂”过程中加入的沉淀剂为饱和的___(化学式)溶液。
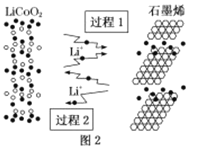
(2)利用锂离子能在石墨烯表面和电极之间快速大量穿梭运动的特性,开发出石墨烯电池,电池反应式为LiCoO2+C6![]() LixC6+Li1-xCoO2其工作原理如图2。下列关于该电池的说法正确的是___(填字母)。
LixC6+Li1-xCoO2其工作原理如图2。下列关于该电池的说法正确的是___(填字母)。
A.过程1为放电过程
B.该电池若用隔膜可选用质子交换膜
C.石墨烯电池的优点是提高电池的储锂容量进而提高能量密度
D.充电时,LiCoO2极发生的电极反应为LiCoO2-xe-=xLi++Li1-xCoO2
E.对废旧的该电池进行“放电处理”让Li+嵌入石墨烯中而有利于回收
(3)LiFePO4也是一种电动汽车电池的电极材料,实验室先将绿矾溶解在磷酸中,再加入氢氧化钠和次氯酸钠溶液反应获得FePO4固体。再将FePO4固体与H2C2O4和LiOH反应即可获得LiFePO4同时获得两种气体。
①写出FePO4固体与H2C2O4和LiOH反应溶液获得LiFePO4的化学方程式___。
②LiFePO4需要在高温下成型才能作为电极,高温成型时要加入少量活性炭黑,其作用是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某种有机物A的质谱图和红外光谱图如图,以下说法正确的是( )
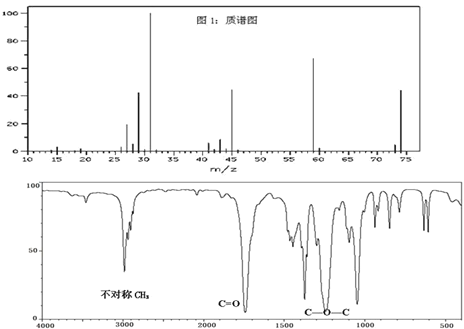
A.由质谱图可知,有机物A的摩尔质量为74
B.由红外光谱可知,有机物A的分子式C3H6O2
C.有机物A的核磁共振氢谱图中有3种吸收峰,峰面积之比为1:2:3
D.有机物A的名称为甲酸乙酯,官能团为酯基
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com