
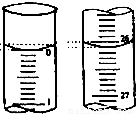
 ,分析不当操作对V(标准)×的影响,以此判断浓度的误差;
,分析不当操作对V(标准)×的影响,以此判断浓度的误差;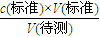 ,可知c(标准)偏大,
,可知c(标准)偏大,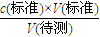 ,可知c(标准)不变,
,可知c(标准)不变, ,可知c(标准)偏大,故C错误;
,可知c(标准)偏大,故C错误; ,可知c(标准)偏小,故D正确;
,可知c(标准)偏小,故D正确;

 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:阅读理解
| ||
| ||
| ||
| 实验现象 | 原因 |
| 溶液最初从紫色逐渐变为 红 红 色 |
氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | 氯气与水反应生成的HClO将石蕊氧化为无色物质 氯气与水反应生成的HClO将石蕊氧化为无色物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某同学欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂.请回答下列问题:
某同学欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
某同学欲用已知物质的量浓度的HCl溶液滴定未知浓度的NaOH溶液时,选择酚酞作指示剂。请回答下列问题:
(1)该同学的实验操作过程如下:
A.取一支碱式滴定管,用蒸馏水洗净
B.加入待测的NaOH溶液,记录液面刻度读数
C.用酸式滴定管精确放出一定量标准液,置于未经标准液润洗的洁净的锥形瓶中
D.在锥形瓶中加入2滴酚酞试液
E.滴定时,边滴加边振荡,同时还要注视滴定管内液面的变化
F.当小心滴到溶液由无色变成粉红色时,30s内不变色即停止滴定
G.记录液面刻度读数
H.据滴定管的两次读数得出所用NaOH溶液的体积为22mL
上述实验过程中有错误的是__________(填编号,下同)。
(2)下列操作可能使所测NaOH溶液浓度偏低的有___________。
A.酸式滴定管洗净后,不经标准HCl溶液润洗就直接使用
B.滴定前锥形瓶用蒸馏水洗净后未经干燥
C.酸式滴定管漏液
D.对碱式滴定管读数时,开始时平视,结束时仰视
E.滴定过程中,由于振荡锥形瓶过于激烈,使少量溶液溅出瓶外
(3)另一同学用0.2010mol/L标准盐酸滴定待测烧碱溶液,根据下表数据,计算待测烧碱溶液的浓度为_______。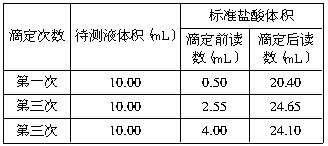
(4)常温时,若用0.1mol/L的NaOH溶液滴定25mL0.1mol/L的盐酸,至终点时不慎少滴加了一滴(每一滴溶液约0.05mL)NaOH溶液,终点时溶液的pH=_____;若不慎多滴加了一滴NaOH溶液,终点时溶液的pH=_______。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
已知醋酸和盐酸是日常生活中极为常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH ![]() CH3COO-+H+ ;ΔH>0
CH3COO-+H+ ;ΔH>0
(1)25 ℃时,浓度均为0.1mol/L的盐酸和醋酸溶液,下列说法正确的是 ;
①两溶液的pH相同
②两溶液的导电能力相同
③由水电离出的c(OH-)相同
 ④中和等物质的量的NaOH溶液,消耗两溶液的体积相同
④中和等物质的量的NaOH溶液,消耗两溶液的体积相同
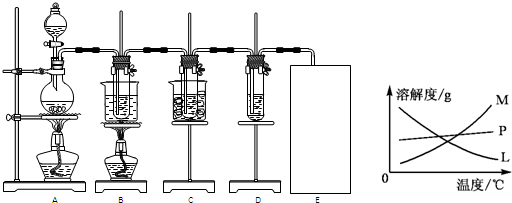
(2)25 ℃时,向pH均为1的盐酸和醋酸溶液中分别加水,随加水
量的增多,两溶液pH的变化如图所示,则符合盐酸pH变化
的曲线是 ;
(3)25 ℃时,向体积为Va mL pH=3的醋酸溶液中滴加pH=11的
NaOH溶液Vb mL至溶液恰好呈中性,则Va Vb(填“>”、“<”或“=”)
假设质检部门规定市售醋酸浓度不得低于4.8g/100mL,某同学欲用中和滴定的方法来测定某品牌的食用醋中的醋酸含量是否达标。实验具体步骤如下:①托盘天平称取一定质量NaOH并配制成500mL NaOH溶液;②用已知浓度的盐酸标准溶液准确标定该NaOH溶液的浓度;③用上述已知准确浓度的NaOH溶液测定醋酸的浓度。
(4)不直接用配置的NaOH溶液滴定样品,而要用标准盐酸先标定再滴定的原因是 ;
(5)若实验过程如下:准确量取该食用醋20.00mL,置于250mL锥形瓶中,再滴加酚酞指示剂,用标定好的0.1000mol/L的NaOH溶液滴定,酚酞指示剂由 色恰好变成__________色且 即为终点。
重复滴定多次,结果记录如下:
| 测定次序 | 第一次 | 第二次 | 第三次 | 第四次 |
| V(mL) | 19.40 | 15.10 | 14.90 | 15.00 |
则该食用醋中醋酸的物质的量浓度=________ mol·L-1,是否合格 (填”是”或”否”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com