
| A. | ②和④ | B. | ①和③ | C. | ①和② | D. | ①和④ |
科目:高中化学 来源: 题型:解答题
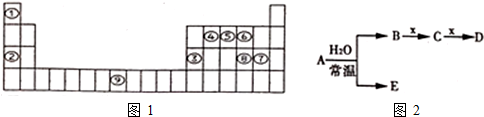
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知C2H2(g)+$\frac{5}{2}$O2(g)→2CO2(g)+H2O(l)△H=-1300KJ/mol 当有5NA个电子转移时能放出650KJ的热量 | |
| B. | 有28g乙烯与丙烯混合气体,其含原子总数为3NA个 | |
| C. | 有反应H2(g)+I2(g)?2HI(g)△H=-QHJ/mol在298K 101KPa下向一密闭容器中充入NA个H2和NA个I2,充分反应共放出热量为QKJ | |
| D. | 在78g苯中含3NA个碳碳双键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度(K) | 平衡时NH3的物质的量(mol) |
| T1 | 2.4 |
| T2 | 2.0 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | |
| Z | W |
| A. | 四种短周期元素中W的原子半径最小 | |
| B. | Z元素在周期表中的位置是第三周期第ⅣA族 | |
| C. | 原子最外层电子数由多到少的顺序:Y>X>W>Z,最高正价由高到低顺序:W>Z | |
| D. | 元素非金属性由强到弱的顺序:W>Z,W的单质常温下可与氢氧化钠溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 甲 | 乙 | |
| 丙 | 丁 | 戊 |
| A. | 原子半径:甲<乙,简单阴离子的半径:丙>丁>戊 | |
| B. | 非金属性:乙<丁 | |
| C. | 最高价氧化物对应的水化物的酸性:丙<丁 | |
| D. | 气态氢化物的稳定性:丙>丁>戊 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高二上第一次月考化学卷(解析版) 题型:选择题
只改变一个影响因素,平衡常数K与化学平衡移动的关系叙述错误的是( )
A.K值不变,平衡可能移动 B.K值变化,平衡一定移动
C.平衡移动,K值可能不变 D.平衡移动,K值一定变化
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol甲醇中含有C-H键的数目为4NA | |
| B. | 25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA | |
| C. | 0.1mol的CaC2中含阴离子数是0.1NA | |
| D. | 1L 0.1mol•L-1的NaHCO3溶液中HCO${\;}_{3}^{-}$和CO${\;}_{3}^{2-}$离子数之和为0.1NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com