
将ag镁铝合金投入到xmL2mol/L的盐酸中,金属完全溶解后,再加入ymL1mol/L的氢氧化钠溶液,得到的沉淀量最大,质量为(a+1.7)g。下列说法不正确的是
A.镁铝合金与盐酸反应转移电子总数为0.1NA
B.x=2y
C.沉淀是Mg(OH)2和Al(OH)3的混合物
D.2x=y
科目:高中化学 来源:2015-2016学年河北省高二上学期第二次月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)═4Fe(OH)3(s)能自发进行,则△H<0
B.铁片镀锌时,铁片与外电源的正极相连
C.以熔融Al2O3为电解质进行电解冶炼铝,熔融体中Al3+向阳极移动
D.t℃时,恒容密闭容器中反应:NO2(g)+SO2(g)?NO(g)+SO3(g),通入少量O2, 的值及SO2转化率不变
的值及SO2转化率不变
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二上学期第一次月考化学试卷(解析版) 题型:填空题
(14 分,每空 2 分)下表是稀硫酸与某金属反应的实验数据:
实验 | 金属 | 金属 | C(H2SO4) | V(H2SO4) | 溶液温度/℃ | 金属消失 | |
序号 | 质量/g | 状态 | /mol·L-1 | /mL | 反应前 | 反应后 | 的时间/s |
1 | 0.10 | 丝 | 0.5 | 50 | 20 | 34 | 500 |
2 | 0.10 | 粉末 | 0.5 | 50 | 20 | 35 | 50 |
3 | 0.10 | 丝 | 0.7 | 50 | 20 | 36 | 250 |
4 | 0.10 | 丝 | 0.8 | 50 | 20 | 35 | 200 |
5 | 0.10 | 粉末 | 0.8 | 50 | 20 | 36 | 25 |
6 | 0.10 | 丝 | 1.0 | 50 | 20 | 35 | 125 |
7 | 0.10 | 丝 | 1.0 | 50 | 35 | 50 | 50 |
8 | 0.10 | 丝 | 1.1 | 50 | 20 | 34 | 100 |
9 | 0.10 | 丝 | 1.1 | 50 | 30 | 44 | 40 |
分析上述数据,回答下列问题:
(1)实验 4 和 5 表明,___________对反应速率有影响,____________反应速率越快,能表明同一规律的实验还有____________(填实验序号);
(2)仅表明反应物浓度对反应速率产生影响的实验有 ____ (填实验序号);
(3)本实验中影响反应速率的其他因素还有 ________ ,其实验序号是 ____ 。
(4)实验中的所有反应,反应前后溶液的温度变化值(约 15℃)相近,推测其原因: 。
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三上学期10月月考化学试卷(解析版) 题型:选择题
可逆反应①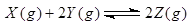 、②
、②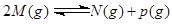 分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密闭隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密闭隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
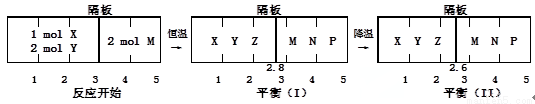
下列判断正确的是:
A.反应①的正反应是吸热反应
B.达平衡(I)时体系的压强与反应开始时体系的压强之比为14:15
C.达平衡(I)时X的转化率为5/11
D.在平衡(I)和平衡(II)中的M的体积分数相同
查看答案和解析>>
科目:高中化学 来源:2016届湖南省常德市高三上学期10月月考化学试卷(解析版) 题型:填空题
(6分)酸性KMnO4、H2O2、NaClO在生产、生活、卫生医疗中常用作消毒剂,其中H2O2还可用于漂白,是化学实验室里必备的重要氧化试剂。高锰酸钾造成的污渍可用还原性的草酸(H2C2O4)去除,Fe(NO3)3也是重要氧化试剂,下面是对这三种氧化剂性质的探究。
(1)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,写出该反应的化学方程式并用双线桥法在化学方程式上标出电子转移的方向和总数____________________。
(2)取300mL0.2mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的物质的量的是________mol。
(3)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色。写出溶液先变为浅绿色的离子方程式_________________________________。
查看答案和解析>>
科目:高中化学 来源:2016届湖南省浏阳市高三上学期第二次月考化学试卷(解析版) 题型:实验题
(12分)某学生为了探究钠与CO2的反应,利用如图装置进行实验。(已知PdCl2能被CO还原得到黑色的Pd)
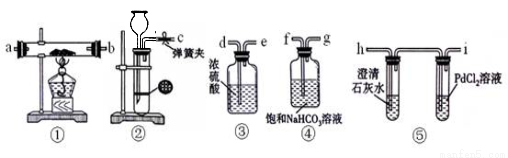
(1)请将上图各装置连接完整(填写装置中字母):c接f, 接 , 接 , 接 。
(2)若用稀盐酸与CaCO3反应制备CO2,在加稀盐酸时,发现CaCO3与稀盐酸不能接触,而稀盐酸又不够了,为使反应能顺利进行,可向长颈漏斗中加入的试剂是 。
A.H2SO4溶液 B.CCl4 C.苯 D.稀硝酸
(3)检查装置气密性并装好药品后,点燃酒精灯之前应进行的操作是打开弹簧夹,让CO2充满整个装置,当观察到 时再点燃酒精灯。
(4)若反应过程中CO2足量,探究钠与CO2充分反应后,生成的固体物质的可能的情况,某同学提出以下猜想:
①生成的固体物质为Na2CO3
②生成的固体物质为Na2CO3和C的混合物
③生成的固体物质为Na2CO3和Na2O的混合物
④生成的固体物质为Na2O和C的混合物
你认为正确的是 (填序号)。
假如反应过程中有下列两种情况,分别写出两种情况下钠与CO2反应的化学方程式。
Ⅰ.装置⑤PdCl2溶液中观察到有黑色沉淀,装置①中固体成分只有一种,且向固体中加入稀盐酸产生能使澄清石灰水变浑浊的气体: ;
Ⅱ.装置①中钠的质量为0.46g,充分反应后,将装置①中的固体加入到足量稀盐酸中产生224mL(标准状况)CO2气体,且溶液中还有固体残留: 。
查看答案和解析>>
科目:高中化学 来源:2016届湖南省长沙市高三上学期第三次月考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列叙述正确的是
A.常温时56g铁片投入足量浓硫酸中生成NA个SO2分子
B.12 g石墨和C60的混合物中质子总数一定为6NA个
C.25℃,pH=12的Na2CO3溶液中含有CO32-的数目为0.01NA
D.氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高一上学期第一次月考化学试卷(解析版) 题型:选择题
已知1.505×1023个X气体分子的质量为8g,则X气体的摩尔质量是
A.16g B.32g C.64g /mol D.32g /mol
查看答案和解析>>
科目:高中化学 来源:2016届山东省淄博市高三上学期10月月考化学试卷(解析版) 题型:选择题
下列化学实验事实及其结论都正确的是
选项 | 实验事实 | 结论 |
A | 将SO2通入含HClO的溶液中生成H2SO4 | HClO的酸性比H2SO4强 |
B | 铝箔在酒精灯火焰上加热熔化但不滴落 | 铝箔表面氧化铝熔点高于铝 |
C | 将水蒸气通过灼热的铁粉,粉末变红 | 铁与水在高温下发生反应 |
D | 将铜丝插入浓硫酸中加热,有气泡冒出 | Cu与浓硫酸发生置换反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com