
【题目】下图中的实验装置可以用于实验室制取乙炔。请填空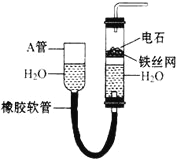
(1)图中,A管的作用是____________。制取乙炔的化学反应方程式为____________。
(2)乙炔通入酸性KMnO4溶液中,发生____________反应,可以观察到____________现象。
(3)乙炔燃烧的化学方程式为________________________,点燃乙炔前应该先________________________。
【答案】 调节水面的高度来控制反应的发生和停止 CaC2+2H2O→Ca(OH)2+CH≡CH↑ 氧化 紫色酸性高锰酸钾溶液逐渐褪色 2CH≡CH+5O2![]() 4CO2+2H2O 验纯
4CO2+2H2O 验纯
【解析】(1)图示装置可通过调节A管的高度,控制反应的发生和停止:将A管提高,右管中水面上升,与电石接触发生反应;将A管降低,右管中水面下降,水与电石脱离接触,反应停止,则制取乙炔的化学反应方程式为CaC2+2H2O→Ca(OH)2+CH≡CH↑;
(2)乙炔容易被高锰酸钾氧化,使高锰酸钾褪色;能够和溴水发生加成反应;
(3)乙炔燃烧的化学方程式为 2CH≡CH+5O2 ![]() 4CO2+2H2O;乙炔中含碳的质量分数较大,燃烧时火焰明亮并伴有浓烈的黑烟;乙炔点燃前必须检验其纯度。
4CO2+2H2O;乙炔中含碳的质量分数较大,燃烧时火焰明亮并伴有浓烈的黑烟;乙炔点燃前必须检验其纯度。


科目:高中化学 来源: 题型:
【题目】右图是周期表中短周期的一部分。若X原子最外层电子数比次外层电子数少3个,则下列说法中不正确的是( )

A. 原子半径的大小顺序是Z>Y>X>W
B. Z的气态氢化物比X的气态氢化物稳定
C. X、Y、Z各元素最高价和最低价的绝对值之和为8
D. X、Y、Z最高价氧化物对应水化物的酸性强弱关系Z>Y>X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中A与B反应生成C,其反应速率分别用v(A)、v(B)、v(C)表示。已知v(A)、v(B)、v(C)之间有以下关系:2v(A)=3v(B),v(C)=2v(B),则此反应可表示为
A.3A+2B=4C B.2A+3B=6C C.3A+2B=C D.2A+3B=4C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)海水中的钠盐、镁盐等都是重要的化工原料,从海水中提取铀、重水对一个国家来说具有战略意义。
①写出氯化镁的电子式__________________________
②重水的摩尔质量为____________________________
③写出金属镁的工业冶炼方程式_____________________
④海水淡化的常见方法有电渗析法、离子交换法、_________________
(2)比赛中,当运动员肌肉挫伤或扭伤时,随队医生即对准受伤部位喷射氯乙烷(沸点12.27℃)进行局部冷冻麻醉应急处理。
①乙烯和氯化氢在一定条件下反应的化学方程式是____________________________
②决定氯乙烷能用于冷冻麻醉应急处理的具体性质是________(填选项)
A.沸点低 B.沸点高 C.易挥发 D.难挥发
③甲烷与氯气光照下反应生成产物共________种
(3)“可燃冰”是天然气与水相互作用形成的晶体物质,若把“可燃冰”(用甲烷表示)燃烧在一定条件下改装成原电池,则在原电池的负极发生反应的物质是__________________________
四、解答题
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,体积均为0.25 L的三个恒容密闭容器中发生可逆反应:N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ·mol-1,达到平衡。下列说法正确的是( )
2NH3(g) ΔH=-92.4 kJ·mol-1,达到平衡。下列说法正确的是( )
容器编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | ||
N2 | H2 | NH3 | NH3 | ||
① | 500 | 1 | 3 | 0 | 0.5 |
② | 500 | 0.6 | 1.8 | 0 | |
③ | 550 | 0 | 0 | 2 | a |
A. 容器①、②中反应的平衡常数不相等
B. 达平衡时,容器②中H2的转化率大于25%
C. a<0.5
D. 起始时向容器①中充入1 mol N2、2 mol H2、0.5 mol NH3,则反应将向逆反应方向进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烟气中含有氮氧化物(NOx),必须除去(即脱硝)后才能排放。
(1) C2H4可用于烟气脱硝。图1为在其他条件一定时,温度、催化剂中Cu2+负载量对NOx去除率的影响。为达到最高的NOx去除率,应选择的反应温度和Cu2+负载量分别是________、________。

图1
(2) 臭氧也可用于烟气脱硝。O3氧化NO结合水洗,可产生HNO3和O2,该反应的化学方程式为______________________。
(3) 图2是用NH3脱除烟气中NO的原理。
①该脱硝原理中,NO最终转化为________(填化学式)和H2O。
②当消耗2 mol NH3和0.5 mol O2时,除去的NO在标准状况下的体积为________ L。

(4) 用碱液脱硝是目前研究的课题之一。
①将NO、NO2通入石灰乳中可制备重要的工业原料Ca(NO2)2。该工艺需控制NO和NO2物质的量之比接近1∶1。若n(NO2)∶n(NO)>1∶1,则会导致________;若n(NO2)∶n(NO)<1∶1,则会导致________。
②将氢氧化钠溶液脱硝得到的NaNO2、NaNO3的混合液和NaOH溶液分别加到图3所示的电解槽中进行电解。A室NO发生的电极反应是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列观点你不赞成的是
A.氢气让人欢喜让人忧
B.煤为人类提供能源和化工原料的同时,也埋下了祸根
C.煤气化能提高市民的生活质量,同时也是潜伏着的无形杀手
D.水虽然是取之不尽的,但个别地区存在用水危机
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由硫铁矿烧渣(主要成分:Fe3O4、Fe2O3、和FeO)得到绿矾(FeSO4·7H2O),在通过绿矾制备铁黄[FeO(OH)]的流程如下:
![]()
已知:FeS2和铁黄均难溶于水
下列说法不正确的是
A. 步骤①,最好用硫酸来溶解烧渣
B. 步骤②,涉及的离子方程式为FeS2+14Fe3++8H2O=15Fe2++2SO42-+16H+
C. 步骤③,将溶液加热到有较多固体析出,再用余热将液体蒸干,可得纯净绿矾
D. 步骤④,反应条件控制不当会使铁黄中混有Fe(OH)3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com