
【题目】用NA表示阿伏加德罗常数,下列说法正确的是
① 18g D2O含有的电子数为10NA;
② 1mol Na2O2与水完全反应时转移电子数为2NA ;
③ 12g石墨烯(单层石墨)中含有六元环的个数为0.5NA;
④ 在标准状况下,22.4LSO3的物质的量为1mol;
⑤ 7.8g过氧化钠中含有的离子数为0.3NA;
⑥ 28g 硅晶体中含有2NA个Si—Si键
⑦ 200mL1mol/LFe2(SO4)3溶液中,Fe3+和SO42-离子数的总和是NA
⑧ 在常温常压下,0.1mol铁与0.1molCl2充分反应,转移的电子数为0.3NA
⑨ 标准状况下,22.4LNO和11.2LO2混合后气体的分子总数为1.5NA
⑩ S2和S8的混合物共6.4g,其中所含硫原子数一定为0.2NA
A、①③⑤⑧ B、②④⑥⑦ C、③⑤⑥⑩ D、⑤⑧⑨⑩
【答案】C
【解析】
试题分析:①D2O的摩尔质量为20g·mol-1,18g重水的含有电子的物质的量为18×10/20mol=9mol,故错误;②2Na2O2+2H2O=4NaOH+O2↑,过氧化钠既是还原剂又是氧化剂,有2mol过氧化钠参加反应共转移电子的物质的量为2mol,因此1mol过氧化钠参加反应,转移电子1mol,故错误;③石墨中一个碳原子被3个环共有,一个六元环真正占有的碳原子为6×1/3=2,12g石墨烯中含有的碳原子为12/12mol=1mol,因此12g石墨烯中含有六元环的个数为0.5NA,故正确;④SO3标准状况下,不是气体,故错误;⑤过氧化钠的阴阳离子个数比为1:2,1moL过氧化钠中含有离子物质的量为3mol,7.8g过氧化钠中含有的离子物质的量为7.8×3/78mol=0.3mol,故正确;⑥硅晶体中一个硅实际占有2个硅硅键,28g硅晶体含有硅硅键的物质的量为28×2/28mol=2mol,故正确;⑦硫酸铁属于强酸弱碱盐,Fe3+要水解,因此两离子的物质的量应小于1mol,故错误;⑧2Fe+3Cl2=2FeCl3,根据量的关系,氯气不足,0.1mol氯气参加反应转移电子0.1×2mol=0.2mol,故错误;⑨2NO+O2=2NO2,2NO2![]() N2O4,分子物质的量应小于1mol,故错误;⑩6.4g是硫原子的质量,因此硫原子的物质的量为6.4/32mol=0.2mol,故正确,因此选项C正确。
N2O4,分子物质的量应小于1mol,故错误;⑩6.4g是硫原子的质量,因此硫原子的物质的量为6.4/32mol=0.2mol,故正确,因此选项C正确。


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:
【题目】关于 F、Cl、Br、I 性质的比较,下列说法不正确的是( )
A. 单质的颜色随核电荷数的增加而加深 B. 沸点:I2 < Br2 < Cl2 <F2
C. 酸性:HIO4< HBrO4 < HClO4 D. 与氢气反应的剧烈程度:I2 < Br2 < Cl2 <F2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知硝酸铵在不同温度下分解会有不同的产物,反应方程式如下,
![]() ①
①
![]() ②
②
![]() ③
③
![]() ④
④
请回答下列问题
(1)这四个反应中属于氧化还原反应的有 ___________个。
(2)反应③中物质X的化学式是 _______________。
(3)反应④中氧化产物和还原产物依次是 ____、____。(填化学式)
(4)若反应③生成标准状况下的11.2L氧气,则转移电子数为 _____ 。
(5)反应②中所得混合气体的平均摩尔质量是 ____________ 。(保留三位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
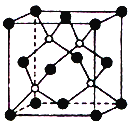
【题目】2013年绵阳科博会场馆,大量的照明材料或屏幕都使用了发光的二极管(LED)。目前市售LED铝片,材质基本以GaAs(砷化镓)、AlGaInP(氮化铟镓)为主。已知砷化镓的晶胞结构如图。试回答:
(1)镓的基态原子的外围电子排布式是_______________。
(2)镓与钾、钙元素的第一电离能从大到小依次为_________________________,与其在同一周期的砷、硒和溴的电负性从大到小依次为_______________。(填元素符号)
(3)此晶胞中所含的砷原子(白色球)个数为_______,与同一个镓原子相连的砷原子构成的立体构型为___________,镓采取的杂化方式为________________。
(4)与镓同主族的元素硼形成的最高价氧化物对应水化物化学式为_____________________,其结构式为_____________,硼酸是_______元酸。
(5)若砷和镓两元素的相对原子质量分别为a,b,GaAs晶体结构图中相距最近的两个原子的距离为dnm,晶胞参数为________cm,NA表示阿伏伽德罗常数,则该晶体的密度为________g/cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸钴是制作氧化钴和金属钴的原料。一种利用含钴废料(主要成分为Co2O3,含少量Fe2O3、Al2O3、CaO、MgO、碳及有机物等)制取CoC2O4的工艺流程如下::

(1)“550℃焙烧”的目的是______________________;
(2)“浸出液”的主要成分是_____________________;
(3)“钴浸出”过程中Co3+转化为Co2+,反应的离子方程式为_____________________;
(4)“净化除杂1”过程中,先在40 ~ 50℃加入H2O2,其作用是___________________________(用离子方程式表示);再升温至80 ~ 85℃,加入Na2CO3溶液,调pH至4.5,“滤渣1”主要成分的是
_____________________。
(5)“净化除杂2”可将钙、镁离子转化为沉淀过滤除去,若所得滤液中c(Ca2+)=1.0×l0-5mol /L,则滤液中 c(Mg2+)为________________ [已知Ksp(MgF2) =7.35×10-11、Ksp(CaF2) =1.05×10-10]。
(6)为测定制得样品的纯度,现称取1.00 g样品,将其用适当试剂转化,得到草酸铵[(NH4)2C2O4]溶液,再用过量稀硫酸酸化,用0. 1000 mol/L KMnO4溶液滴定,达到滴定终点时,共用去KMnO4溶液26.00 mL,则草酸钴样品的纯度为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知SO32-的还原性大于I-的还原性,某无色溶液中可能含有I-、NH4+、Cu2+、SO32-,向该溶液中加入少量溴水,溶液仍呈无色,则下列关于溶液组成的判断正确的是
①肯定不含I-;②肯定不含Cu2+;③肯定含有SO32-;④可能含有I-
A. ①③ B. ①②③ C. ③④ D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,属于氧化还原反应同时又是吸热反应的是()
A. Ba(OH)2·8H2O与NH4Cl反应
B. 铝与稀盐酸
C. 灼热的炭与水蒸气生成一氧化碳和氢气的反应
D. 煤与O2的燃烧反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列物质在水溶液中的电离方程式:
(1)Ba(OH)2:_______________________________________。
(2)KHSO4:________________________________________。
(3)HNO3:_________________________________________。
(4)Na2CO3:_______________________________________。
(5)NaHCO3:_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸氯(C1NO)是有机合成中的重要试剂。可由NO与Cl2在通常条件下反应得到,化学方程式为2NO(g)+C12(g)![]() 2C1NO(g)。
2C1NO(g)。
(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酸氯,涉及如下反应:
①2NO2(g)+NaC1(s)![]() NaNO3(s)+ClNO(g) K1
NaNO3(s)+ClNO(g) K1
②4NO2(g)+2NaC1(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g) K2
2NaNO3(s)+2NO(g)+Cl2(g) K2
③2NO(g)+C12(g)![]() 2C1NO(g) K3
2C1NO(g) K3
则K1,K2,K3之间的关系为K3=______________。
(2)已知几种化学键的键能数据如下表(亚硝酸氯的结构为Cl-N=O):

则2NO(g)+C12(g)![]() 2C1NO(g)反应的ΔH和a的关系为ΔH =_____________kJ/mol。
2C1NO(g)反应的ΔH和a的关系为ΔH =_____________kJ/mol。
(3)300℃时,2NO(g)+C12(g)![]() 2ClNO(g)的正反应速率表达式为v正 = k·cn(ClNO),测得速率和浓度的关系如下表:
2ClNO(g)的正反应速率表达式为v正 = k·cn(ClNO),测得速率和浓度的关系如下表:
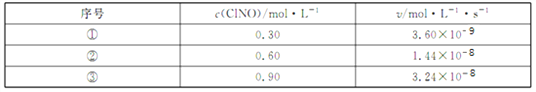
n =____________;k =__________________(注明单位)。
(4)在1L的恒容密闭容器中充入2molNO(g)和1molC12(g),在不同温度下测得c(C1NO)与时间的关系如图A:

①该反应的ΔH ____________0(填“>”、“<”或“=”);
②反应开始到10min时NO的平均反应速率v(NO)=____________mol/(L·min);
③T2时该反应的平衡常数K=____________。
(5)一定条件下在恒温恒容的密闭容器中按一定比例充入NO(g)和Cl2(g),平衡时ClNO的体积分数随n(NO)/n(C12)的变化图象如图B,则A、B、C三状态中,NO的转化率最大的是____________点,当n(NO)/n(C12)=1.5时,达到平衡状态ClNO的体积分数可能是D、E、F三点中的____________点。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com