
 ��þ�����Ļ���ﹲ0.2mol������200mL 4mol•L-1��������Һ�У�Ȼ���ٵμ�2mol•L-1��NaOH��Һ��
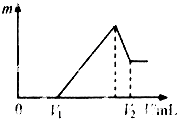
��þ�����Ļ���ﹲ0.2mol������200mL 4mol•L-1��������Һ�У�Ȼ���ٵμ�2mol•L-1��NaOH��Һ������ ��1������ͼ���֪���ڵμ�NaOH��Һ�����V1=160mL�����У�û�г������ɣ�˵��������ʣ�࣬�μӵ�NaOH�����к�ʣ�����ᣬV1=160mLʱ��ʣ���HCl��μӵ�NaOHǡ����ȫ��Ӧ����Һ��MgCl2��AlCl3��NaCl���Һ������Mgԭ�ӡ�Alԭ�ӡ�Cl-���ӡ�Na+�����غ㣬�з�������n��Al����
��2������Һ��Mg2+��Al3+ǡ�ó�����ȫʱ���������ﵽ���ֵ����ʱ����Һ��NaCl��Һ������Cl-���Ӻ�Na+�����غ���n��Na+��=n��NaCl��=��HCl�����n��NaOH����������V=$\frac{n}{c}$�������NaOH��Һ�������
��3����Ӧ��Ļ����Һ���ټ�840mL 2mol•L-1��NaOH��Һ�����ó�������Al��OH��3������Ϊ�����ơ�ƫ�����ƣ�����Ϊ����������a��1�������������غ㣬Ӧ����n��NaOH����2n��Na2SO4��+n��NaAlO2����������Ԫ���غ���a��ʾ��n��NaAlO2�����ݴ�ȷ��a��ȡֵ��Χ��
��� �⣺��1����V1=160mLʱ����ʱ����Һ��MgCl2��AlCl3��NaCl�Ļ��Һ��
��Na+�����غ��֪��n��NaCl��=n��Na+��=n��NaOH��=0.16L��2mol/L=0.32mol��
200mL 4mol•L-1��������Һ�к����Ȼ�������ʵ���Ϊ��4mol/L��0.2L=0.8mol��
�������к���MgCl2xmol��AlCl3Ϊymol����
����Mgԭ�ӡ�Alԭ���غ��У�x+y=0.2��
����Cl-�����غ��У�2x+3y=0.8-0.32=0.48��
�������̽�ã�x=0.12��y=0.08��
���Խ�����ĩ�У�n��Mg��=0.12mol��n��Al��=y=0.08mol��
�𣺽�����ĩ���������ʵ���Ϊ0.08��
��2������Һ��Mg2+��Al3+ǡ�ó�����ȫʱ����ʱ����Һ��NaCl��Һ������Cl-���Ӻ�Na+�����غ��У�n��Na+��=n��NaCl��=��HCl��=4mol/L��0.2L=0.8mol��
������Ҫ��������������Һ���Ϊ��V��NaOH��=$\frac{0.8mol}{2mol/L}$=0.4L=400mL��
�ʴ�Ϊ��400��
��3������Ϊ����������a��1��Al�����ʵ���Ϊ��0.2��1-a��mol����Ӧ��Ļ����Һ���ټ���840mL 2mol•L-1��NaOH��Һ�����ó�������Al��OH��3��������Ϊ�����ơ�ƫ�����ƣ�������Ԫ���غ��֪��n��NaAlO2��=0.2��1-a��mol��
�����������غ㣬Ӧ���㣺n��NaOH����2n��Na2SO4��+n��NaAlO2����
����0.84��2��2��0.2��4+0.2��1-a����
��ã�a��0.6��
����a��ȡֵ��ΧΪ����0.6��a��1��
�ʴ�Ϊ��0.6��a��1��
���� ���⿼�����йػ���ﷴӦ�ļ��㣬��Ŀ�Ѷ��еȣ�����ͼ���⣬Ҫ��ȷÿһ��ͼ�����Ļ�ѧ��Ӧ��֪���յ�����ĺ��弰��Һ�����ʵijɷ֣���Ϸ���ʽ���й�������з�����ע���غ�˼������ã�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ⱥ��ʳ��ˮʱ�������ĵ缫��ӦʽΪ��2Cl--2e-�TCl2�� | |
| B�� | ���������绯ѧ��ʴ��������Ӧʽ��Fe-2e-�TFe2+ | |
| C�� | ��ͭ����ʱ�����Դ�����������Ǵ�ͭ���缫��ӦʽΪ��Cu2++2e-�TCu | |
| D�� | ����ȼ�ϵ�صĸ�����Ӧʽ��O2+2H2O+4e-�T4OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na����ˮ�У��������壺2Na+2H2O�T2Na++2OH-+H2�� | |
| B�� | �ڳ����ʯ��ˮ��ͨ�����SO2��SO2+OH-�THSO3- | |
| C�� | AlƬ������NaOH��Һ��Ӧ���������壺2Al+2OH-+2H2O�T2AlO2-+3H2�� | |
| D�� | ���������Һ��ͨ������SO2���壺Ca2++2ClO-+SO2+H2O�TCaSO3��+2HClO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������


| �ܶȣ�g/cm3�� | �۵㣨�棩 | �е㣨�棩 | �ܽ��� | |
| ������ | 0.96 | 25 | 161 | ������ˮ |
| ����ϩ | 0.81 | -103 | 83 | ������ˮ |
 ��SO2��CO2��ˮ�������������ͨ���Լ���˳���Ǣܢݢ٢ݢڢۣ���ܢݢ٢ݢۢڣ� ������ţ�
��SO2��CO2��ˮ�������������ͨ���Լ���˳���Ǣܢݢ٢ݢڢۣ���ܢݢ٢ݢۢڣ� ������ţ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��״����11.2L��ˮ�к���0.5��NAˮ���� | |
| B�� | 0.1mol•L-1 NaCl��Һ��Na+����ĿΪ0.1NA | |
| C�� | 1mol H2��O2�Ļ�������к�NA������ | |
| D�� | �ڳ��³�ѹ�£�18��ˮ���е�ԭ����Ϊ3NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ȼ������Ҫ�ɷ� | |
| B�� | ������ | |
| C�� | ����ȡ���������ֽṹ | |
| D�� | �������ڹ����������ܷ���ȡ����Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ʯ��ˮ������ķ�Ӧ��OH-+H+�TH2O | |
| B�� | ����þ��ϡ���ᷴӦ��O2-+2H+�TH2O | |
| C�� | ����þ��Һ������������Һ���ϣ�Ba2++SO42-�TBaSO4�� | |
| D�� | ̼�������ϡ�����У�CO32-+2H+�TH2O+CO2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��3���ڷǽ���Ԫ�غ���������Դ�����������ǿ | |
| B�� | HCl��H2S��PH3���ȶ������� | |
| C�� | ��3������������ԭ�Ӻ����Ӱ뾶�����μ�С | |
| D�� | ��MgCl2��Һ�м�������Ʒ���2Na+MgC12�T2NaC1+Mg�����Խ�����Na��Mg |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com