
| A£® | Mg2+”¢Cl-”¢Na+”¢NO3- | B£® | K+”¢Na+”¢NO3-”¢HCO3- | ||
| C£® | Na+”¢Ba2+”¢Cl-”¢NO3- | D£® | Fe3+”¢Na+”¢AlO2-”¢SO42- |
·ÖĪö ¼ÓČėĀĮ·ŪÄܷųöH2µÄČÜŅŗ£¬ĪŖ·ĒŃõ»ÆŠŌĖį»ņĒæ¼īČÜŅŗ£¬øł¾ŻĄė×ÓÖ®¼ä²»ÄܽįŗĻÉś³É³Įµķ”¢ĘųĢ唢Ė®µČ£¬²»ÄÜ·¢ÉśŃõ»Æ»¹Ō·“Ó¦µČ£¬ŌņĄė×Ó“óĮæ¹²“ę£¬ŅŌ“ĖĄ“½ā“š£®
½ā“š ½ā£ŗ¼ÓČėĀĮ·ŪÄܷųöH2µÄČÜŅŗ£¬ĪŖ·ĒŃõ»ÆŠŌĖį»ņĒæ¼īČÜŅŗ£¬
A£®¼īČÜŅŗÖŠ²»ÄÜ“óĮæ“ęŌŚMg2+£¬ĒŅĖįČÜŅŗÖŠAl”¢H+”¢NO3-·¢ÉśŃõ»Æ»¹Ō·“Ó¦²»Éś³ÉĒāĘų£¬¹ŹA²»Ń”£»
B£®Ėį”¢¼īČÜŅŗÖŠ¾ł²»ÄÜ“óĮæ“ęŌŚHCO3-£¬¹ŹB²»Ń”£»
C£®¼īČÜŅŗÖŠøĆ×éĄė×ÓÖ®¼ä²»·“Ó¦£¬æÉ“óĮæ¹²“ę£¬¹ŹCŃ”£»
D£®¼īČÜŅŗÖŠ²»ÄÜ“óĮæ“ęŌŚFe3+£¬ĖįČÜŅŗÖŠ²»ÄÜ“óĮæ“ęŌŚAlO2-£¬¹ŹD²»Ń”£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éĄė×ӵĹ²“ę£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕĻ°ĢāÖŠµÄŠÅĻ¢¼°Ąė×ÓÖ®¼äµÄ·“Ó¦ĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėÓ¦ÓĆÄÜĮ¦µÄ漲飬עŅāø“·Ö½ā·“Ó¦”¢Ńõ»Æ»¹Ō·“Ó¦µÄÅŠ¶Ļ£¬ĢāÄæÄŃ¶Č²»“ó£®


 ĆĻ½ØĘ½Š”ѧ¹ö¶Æ²āŹŌĻµĮŠ“š°ø
ĆĻ½ØĘ½Š”ѧ¹ö¶Æ²āŹŌĻµĮŠ“š°ø »ĘøŌĢģĢģĮ·æŚĖćĢāæØĻµĮŠ“š°ø
»ĘøŌĢģĢģĮ·æŚĖćĢāæØĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
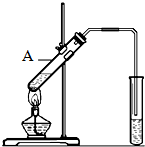 ŅŅĖįŹĒŹ³“×µÄÖ÷ŅŖ³É·Ö£¬Ėü¾ßÓŠŅŌĻĀ»ÆѧŠŌÖŹ£ŗ
ŅŅĖįŹĒŹ³“×µÄÖ÷ŅŖ³É·Ö£¬Ėü¾ßÓŠŅŌĻĀ»ÆѧŠŌÖŹ£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
 ČēĶ¼ŹĒÄ³Ń§Š£ŹµŃéŹŅ“Ó»ÆѧŹŌ¼ĮÉĢµźĀņ»ŲµÄÅØĮņĖįŹŌ¼Į±źĒ©ÉĻµÄ²æ·ÖÄŚČŻ£®
ČēĶ¼ŹĒÄ³Ń§Š£ŹµŃéŹŅ“Ó»ÆѧŹŌ¼ĮÉĢµźĀņ»ŲµÄÅØĮņĖįŹŌ¼Į±źĒ©ÉĻµÄ²æ·ÖÄŚČŻ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µŖŃõ»ÆĀĮÖŠµŖµÄ»ÆŗĻ¼ŪŹĒ-3 | |
| B£® | ·“Ó¦ÖŠŃõ»Æ²śĪļŗĶ»¹Ō²śĪļµÄĪļÖŹµÄĮæÖ®±ČŹĒ1£ŗ2 | |
| C£® | ·“Ó¦ÖŠĆæÉś³É5.7gAlONĶ¬Ź±Éś³É1.12LCO | |
| D£® | AlONŗĶCOµÄ»Æѧ¼üĄąŠĶ²»Ķ¬ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ēå³æµÄŃō¹ā“©¹żĆÆĆܵÄĮÖľ֦Ņ¶Ėł²śÉśµÄĆĄĄö¾°Ļó£ØĆĄĄöµÄ¹āĻߣ© | |
| B£® | Äņ¶¾Ö¢»¼Õߏ¹ÓĆŃŖŅŗĶøĪöÖĪĮĘ | |
| C£® | Ć÷·Æ¾»Ė® | |
| D£® | ĻņFeCl3ČÜŅŗÖŠ¼ÓČėNaOHČÜŅŗ£¬»į³öĻÖŗģŗÖÉ« |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 0.08 | B£® | 0.04 | C£® | 0.032 | D£® | 0.036 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
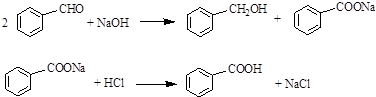
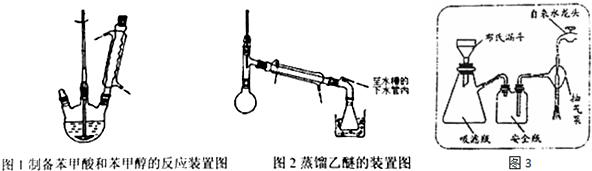
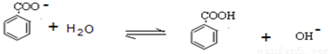 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
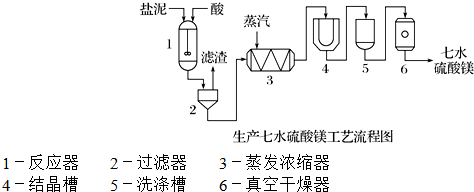
| ³É ·Ö | NaCl | Mg£ØOH£©2 | CaCO3 | BaSO4 | ĘäĖū²»ČÜÓŚĖįµÄĪļÖŹ |
| ÖŹĮæ·ÖŹż/% | 15”«20 | 15”«20 | 5”«10 | 30”«40 | 10”«15 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com