
向200 mL 0.1 mol·L-1 FeCl2溶液中加入适量NaOH,使Fe2+恰好完全沉淀,小心加热此混合物,直到水分蒸干,然后灼烧到质量不再变化,此时固体的质量为( )。
A.1.6 g B.2.34 g
C.3.94 g D.5.00 g
科目:高中化学 来源: 题型:
巴豆酸的结构简式为CH3-CH=CH-COOH。现有①氯化氢;②溴水;③纯碱溶液;④丁醇;⑤酸性高锰酸钾溶液。试根据巴豆酸的结构特点,判断在一定条件下,能与巴豆酸反应的物质是
A.②④⑤ B.①③④ C.①②③④ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于化学反应限度的说法中不正确的是
A.当一个可逆反应达到平衡状态时,就是此反应在该条件下达到的限度
B.当可逆反应进行到平衡状态时,那么这个反应的正向反应速率和逆向反应速率相等
C.平衡状态是一种静止的状态,因为反应物和生成物的浓度已经不再改变
D.化学反应的限度可以通过改变条件而改变
查看答案和解析>>
科目:高中化学 来源: 题型:
金属钛(Ti)性能优越,被称为继铁、铝之后的“第三金属”。工业上以金红石为原料制取Ti的反应 为
为
aTiO2+bCl2+cC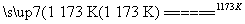 aTiCl4+cCO Ⅰ
aTiCl4+cCO Ⅰ
TiCl4+2Mg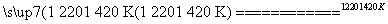 Ti+2MgCl2 Ⅱ
Ti+2MgCl2 Ⅱ
关于反应Ⅰ、Ⅱ的分析不 正确的是 ( )。
正确的是 ( )。
①TiCl4在反应Ⅰ中是还原产物,在反应Ⅱ中是氧化剂;②C、Mg在两个反应中均为还原剂,被还原;
③在反应Ⅰ、Ⅱ中Mg的还原性大于C的,C的还原性大于TiCl4的;④a=1,b=c=2;⑤每生成19.2 g Ti,反应Ⅰ、Ⅱ中共转移 4.8 mol e-。
4.8 mol e-。
A.①②④ B.②③④ C.③④ D.②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
将几滴KSCN(SCN-是“类卤离子”)溶液加入酸性的含有Fe3+的溶液中,溶液变成红色,将该红色溶液分为两份,①一份中加入适量KMnO4溶液,红色退去;②向另一份中通入SO2,红色也退去。下列说法不正确的是 ( )。
A.①红色退去的原因是KMnO4将SCN-氧化,使Fe(SCN)3消失
B.②红色退去的原因是SO2将Fe3+还原为Fe2+
C.②红色退去的原因是SO2将SCN-还原
D.SCN-在适当条件下可失去电子被氧化剂氧化为(SCN)2
查看答案和解析>>
科目:高中化学 来源: 题型:
最新的病毒学研究证实,NO对SARS病毒有直接抑制作用.下列关于NO的叙述正确的( )
A.NO是一种红棕色的气体 B、常温常压下,NO不能与O2直接化合
C.NO可由N2和O2在放电条件下直接化合得到 D、NO易溶于水,不能用排水法收集
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学设计实验证明铜与浓硫酸能发生反应,并检验生成气体的性质,如图所示,在试管里加入2mL浓硫酸,用带导管和一个小孔的胶管塞紧,从孔中插入一根铜丝,加热,把放出的气体依次通入品红溶液和石蕊溶液中。
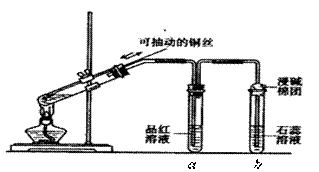
请回答下列问题:
(1)写出铜与浓硫酸反应的化学方程式: 。
(2)试管a、b分别检验生成气体的性质,写出观察到的现象及其作用。
试管a中的现象是 ,作用是 。
试管b中的现象是 ,作用是 。
(3)试管b管口塞一团浸有烧碱溶液的棉花,其作用是 ,
相关的反应是(请写离子方程式) ;
(4)如图用可抽动的铜丝符合化学实验“绿色化”的原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期主族元素X、Y、Z、W、Q的原子序数依次增大,X的气态氢化物极易溶于Y的氢化物中,常温下,Z的单质能溶于W的最高价氧化物的水化物的稀溶液,却不溶于其浓溶液。下列说法不正确的是
A.原子半径的大小顺序为W>Q>Z>X>Y
B.元素X的气态氢化物与Q的单质可发生置换反应
C.元素X与Y可以形成5种以上的化合物
D.元素Q的最高价氧化物对应的水化物酸性比W的强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com