
| A. | 灼热的炭与CO2的反应 | B. | 铝片与稀盐酸的反应 | ||
| C. | Ba(OH)2•8H2O和NH4Cl的反应 | D. | 甲烷在氧气中的燃烧反应 |
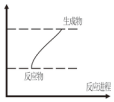
分析 由图可知反应物总能量小于生成物总能量,则应为吸热反应,如发生氧化还原反应,应存在元素化合价的变化,以此解答该题.
解答 解:A.灼热的木炭与CO2反应为吸热反应,C元素的化合价变化,为氧化还原反应,故A正确;
B.金属与盐酸的反应放热,Al、H元素的化合价变化,为氧化还原反应,故B错误;
C.Ba(OH)2•8H2O晶体与NH4Cl晶体的反应为吸热反应,但没有元素的化合价变化,为非氧化还原反应,故C错误;
D.甲烷在氧气中的燃烧反应为放热反应,故D错误.
故选A.
点评 本题考查氧化还原反应及反应中能量变化,为高频考点,把握反应中元素的化合价变化及能量变化为解答的关键,题目难度不大.


科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S→SO2→SO3→H2SO4 | B. | Fe→FeCl2→Fe(OH)2→Fe(OH)3 | ||
| C. | Al→Al2O3→Al(OH)3→NaAlO2 | D. | N2→NO→NO2→HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电子云表示电子在核外单位体积的空间出现的机会多少 | |
| B. | 同一原子处于激发态时的能量一定高于基态时的能量 | |
| C. | 各能级包含的原子轨道数按s、p、d、f的顺序依次为1、3、5、7 | |
| D. | 1个原子轨道里最多只能容纳2个电子,且自旋方向相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Ba2+、NO3-、Cl- | B. | K+、Na+、H+、Cl- | ||
| C. | K+、NH4+、S2-、CO32- | D. | Cu2+、Na+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol•L-1) | 0.64 | 0.50 | 0.50 |
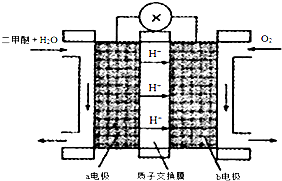
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
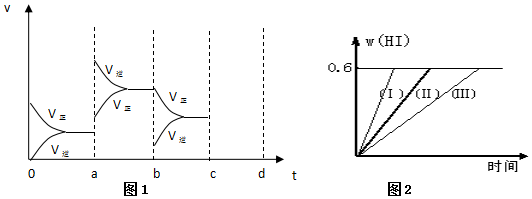
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com