
四种元素X、Y、Z、W位于元素周期表的前四周期,已知它们的核电荷数依次增加,且核电荷数之和为51;Y原子的L层p轨道中有2个电子;Z与Y原子的价层电子数相同;W原子的L层电子数与最外层电子数之比为4︰1,其d轨道中的电子数与最外层电子数之比为5︰1。
(1)Z与X形成只含一个中心原子的共价化合物,则它的分子式是 ,其分子的立体结构是 。
(2)Y的最高价氧化物晶体类型是 晶体。X的氧化物与Y的最高氧化物中,分子极性较小的是(填分子式) 。
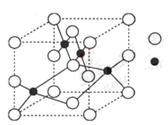
(3)右图是W的某种氧化物的晶胞结构示意图,可确定该晶胞中阴离子的个数为 。(图中实心球表示W元素)
(4)铜元素和W元素都位于周期表的ds区,胆矾
CuSO4·5H2O可写成[Cu(H2O)4]SO4 ·H2O,其结构示意图如右,有关它的说法正确的是 ________(填字母)。
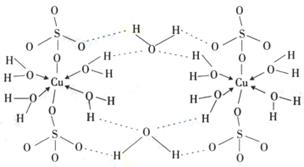
A.该胆矾晶体中存在配位键、共价键和离子键
B.该结构中还存在金属键,极性共价键
C.胆矾是分子晶体,分子间存在氢键
D.胆矾中的水在不同温度下会分步失去
(5)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的空间构型都是三角锥形,单NF3不易与Cu2+形成配离子,其原因是 。
【知识点】分子结构、晶胞计算、化学键配合物
【答案解析】(1) SiH4 正四面体 (各1分)
(2)分子 CO2 (各1分)
(3) 4 (2分)
(4) AD (2分)
(5) NF3分子中氟原子非金属性强是吸电子的,使得氮原子上的孤对电子难于与Cu2+形成配位键。(2分)
解析:Y原子的L层p轨道中有2个电子,所以其核外电子排布式为1s22s22p2,为6号元素碳;Z与Y原子的价电子数相同,最外层为四个电子且均位于元素周期表的前四周期,为14号元素硅;W原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:1,所以其核外电子排布式为1s22s22p63s23p63d104s2,为30号锌元素;电荷数之和为51,51-30-6-14=1,则X的原子序数是1,是元素氢。
(1)Si与H形成只含一个中心原子的共价化合物SiH4,硅烷分子中含有4个σ键不含孤电子对,所以都是采取sp3杂化,立体构型是正四面体构型;(2)Y元素最高价氧化物为二氧化碳,晶体类型为分子晶体;X的氧化物是水,水是极性分子,二氧化碳是非极性分子,所以分子极性较小的是CO2;(3)从图中可以看出阴离子在晶胞有四类:顶点(8个)、棱上(4个)、面上(2个)、体心(1个),根据立方体的分摊法,可知该晶胞中阴离子数目为:8×1/8 +4×1/4 +2×1/2 +1=4;(4)A.在上述结构示意图中,存在O→Cu配位键,H-O、S-O共价键和Cu、O离子键,故A正确;B.在上述结构示意图中,存在极性共价键,不存在金属键,故B错误;C.胆矾是五水硫酸铜,胆矾是由水合铜离子及硫酸根离子构成的,属于离子晶体,故C错误;D.由于胆矾晶体中水两类,一类是形成配体的水分子,一类是形成氢键的水分子,结合上有着不同,因此受热时也会因温度不同而得到不同的产物,故D正确;(5)N、F、H三种元素的电负性:F>N>H,所以NH3中共用电子对偏向N,而在NF3中,共用电子对偏向F,偏离N原子,导致NF3中N原子的孤对电子难以形成配位键,故NF3不易与Cu2+形成配离子。
【思路点拨】本题以元素的推断为载体考查了核外电子排布式的书写、分子中原子杂化方式的判断等知识点,离子晶体的晶胞结构、化学键、物质性质、配合物成键状况的了解,题目难度中等,学习中注意加强对晶胞以及晶体结构的分析。


科目:高中化学 来源: 题型:
工业催化剂K3[Fe(C2O4)3]·3H2O是翠绿色晶体,在421~553℃时,分解为Fe2O3、K2CO3、CO、CO2、H2O。实验室由草酸亚铁晶体(FeC2O4·2H2O)、草酸钾(K2C2O4)、草酸(H2C2O4)和双氧水(H2O2)混合制备:
2FeC2O4·2H2O + H2O2+ 3K2C2O4+ H2C2O4=2K3[Fe(C2O4)3]·3H2O
(1)[Fe(C2O4)3]3-的名称是_______________。
(2)制备过程要防止草酸被H2O2氧化,写出草酸被H2O2氧化的化学方程式_________。
(3)配合物的稳定性可以用稳定常数K来衡量,如Cu2+ + 4NH3 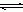 [Cu(NH3)4]2+,其稳定常数表达式为:
[Cu(NH3)4]2+,其稳定常数表达式为: 。已知K [Fe(C2O4)3]3-=1020,K [Fe(SCN)3]= 2×103,能否用KSCN溶液检验K3[Fe(C2O4)3]·3H2O中的铁元素? (填“是”、“否”)。 若选“否”,请设计检验K3[Fe(C2O4)3]·3H2O中铁元素的方案。__________________________。
。已知K [Fe(C2O4)3]3-=1020,K [Fe(SCN)3]= 2×103,能否用KSCN溶液检验K3[Fe(C2O4)3]·3H2O中的铁元素? (填“是”、“否”)。 若选“否”,请设计检验K3[Fe(C2O4)3]·3H2O中铁元素的方案。__________________________。
(4)铁元素可形成多种配合物,其中一种配合物钾盐A是有争议的食品添加剂。经组成分析A仅含K、Fe、C、N四种元素。取36.8g A加热至400℃,分解成KCN、Fe3C、C、N2,生成的氮气折合成标准状况下的体积为2.24L,Fe3C质量是C质量的3倍,Fe3C物质的量是氮气物质的量的1/3。则A的化学式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某混合物X由Al2O3、Fe2O3、Cu、SiO2中的一种或几
种物质组成。某校课外兴趣小组以两条途径分别对X进行如下实验探究:
途径a: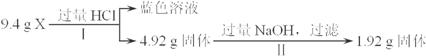
途径b: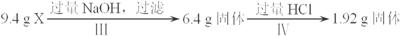
下列有关说法不正确的是( )
A.1.92 g固体只含Cu
B.由Ⅰ可知X中一定存在Fe2O3和Cu
C.原混合物中m(Fe2O3)∶m(Cu)=1∶1
D.原混合物X至少含Al2O3和SiO2中的一种,但不能进一步确认二者的存在与否
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素离子aA2+、bB+、cC3-、dD-都具有相
同电子层结构,则下列叙述正确的是( )
A.原子半径A>B>D>CB.原子序数d>c>b>a
C.离子半径C>D>B>AD.单质还原性A>B>D>C
查看答案和解析>>
科目:高中化学 来源: 题型:
镭是元素周期表中第七周期的ⅡA族元素。下面关于镭的性质的描述中不正确的是( )
A 在化合物中呈+2价 B 单质使水分解、放出氢气
C 氢氧化物呈两性 D 碳酸盐难溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、Q、M为常见的短周期元素,其原子序数依次增大。有关信息如下表:
| X | 动植物生长不可缺少的元素,是蛋白质的重要成分 |
| Y | 地壳中含量居第一位 |
| Z | 短周期中其原子半径最大 |
| Q | 生活中大量使用其合金制品,工业上可用电解其氧化物的方法制备 |
| M | 海水中大量富集的元素之一,其最高正化合价与负价的代数和为6 |
(1)X的气态氢化物的大量生产曾经解决了地球上因粮食不足而导致的饥饿和死亡问题,请写出该气态氢化物的电子式____________。
(2)已知37Rb和53I都位于第五周期,分别与Z和M同一主族。下列有关说法正确的是____________(填序号)。
A.原子半径: Rb>I B.RbM中含有共价键
C.气态氢化物热稳定性:M>I
D.Rb、Q、M的最高价氧化物对应的水化物可以两两发生反应
⑶若XM3最初水解产物是XH3和HMO,则X、M元素的电负性大小顺序是:X_____M((填>、<、或=);若已知磷与M元素电负性关系是:P<M,则PM3水解的化学反应方程式是 。
(4)已知QM3的熔点为190℃(2.02×105Pa),但它在180℃即开始升华,则QM3是_________(填“离子化合物”或“共价化合物”),如何通过实验判别__________________。在500K和1.01×105Pa时,它的蒸气密度(换算成标准状况时)为11.92g/L,则QM3的结构式为_________。
(5)X、Y组成的一种无色气体遇空气变为红棕色。将标准状况下40 L该无色气体与15 L氧气通入一定浓度的NaOH溶液中,恰好被完全吸收,同时生成两种盐。请写出该反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的化学名称、化学式和俗名一致的是( )
A.碳酸钙、CaCO3、生石灰 B.氢氧化钠、NaOH、纯碱
C.碳酸钠、Na2CO3、苏打 D.碳酸氢钠、NaHCO3、苏打
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各化学反应的离子方程式中,有错误的是( )
A.铝与氢氧化钠反应:2Al+2OH-+2H2O=2AlO2-+3 H2↑
B.氧化铝溶于氢氧化钠溶液:Al2O3+2OH-=2AlO2-+H2O
C.碘化亚铁溶液中滴入足量溴水:2Fe2++2I-+2Br2=I2+2Fe3++4Br-
D.碳酸氢镁溶液中加过量澄清石灰水
Mg2++2HCO3-+2Ca2++4OH-=2CaCO3↓+2H2O+Mg(OH)2↓
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com