
【题目】科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z为同一短周期元素,W、Z核外电子数之和是X核外电子数的2倍,Y的最外层电子数是其质子数的![]() 。下列叙述正确的是
。下列叙述正确的是
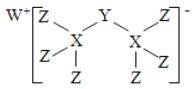
A. X、Z两元素可形成离子化合物
B. 气态氢化物的稳定性:X>Y>Z
C. 该新化合物中的Y元素满足8电子稳定结构
D. Y、Z元素分别对应的最高价氧化物的水化物均是强酸
【答案】C
【解析】
W、X、Y、Z为同一短周期元素,Y的最外层电子数是其质子数的![]() ,Y为Li或P元素,根据化合物的结构示意图,X能形成4个共价键、Z能形成1个共价键,Y能形成2个共价键,则Y只能为P,X位于第IVA族,为Si元素;Z位于第VIIA族,为Cl元素,W、Z核外电子数之和是X核外电子数的2倍, 则W的核外电子数为11,W为Na元素,据此分析解答。
,Y为Li或P元素,根据化合物的结构示意图,X能形成4个共价键、Z能形成1个共价键,Y能形成2个共价键,则Y只能为P,X位于第IVA族,为Si元素;Z位于第VIIA族,为Cl元素,W、Z核外电子数之和是X核外电子数的2倍, 则W的核外电子数为11,W为Na元素,据此分析解答。
根据上述分析可知:W、X、Y、Z分别是Na、Si、P、Cl元素。
A、Si和Cl都是非金属元素,形成共价化合物,故A错误;
B、元素的非金属性越强,气态氢化物越稳定,稳定性:X<Y<Z,故B错误;
C、Y为P元素,其最外层有5个电子,P原子形成2个共价键且该阴离子得到W原子一个电子,所以P原子达到8电子结构,故C正确;
D、磷酸不能完全电离,属于中强酸范畴,不属于强酸,故D错误;
故选C。


 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案科目:高中化学 来源: 题型:
【题目】将一定量的Al、Mg合金加入到足量的40mL某浓度的盐酸中,充分反应后得到标准状况下的氢气896mL;若将等质量的该混合物加入到足量的NaOH溶液中,充分反应后得到标准状况下的氢气672mL。
(1)当合金与盐酸反应时,转移电子总物质的量为_____mol;
(2)合金中Mg的质量为_____g;
(3)合金的平均摩尔质量为_____;
(4)若向与盐酸反应后的溶液中缓慢加入100mL 1mol/L 的NaOH溶液,沉淀质量恰好达到的最大值,则加入盐酸的浓度为_____mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用图表来处理数据是发现科学规律的一种重要方法。
(1)下图是原子序数为1~18的元素原子的最外层电子数随原子序数变化的直方图。图中元素a 是__,b 是____。

(2)下图表示元素的一种性质随原子序数变化的情况,根据分析,该图纵坐标表示的是_________。

(3)下表给出了部分元素的原子半径。
元素符号 | Li | Be | B | C | N | O | F | Na | K | Rb | Cs |
原子半径/nm | 0.152 | 0.089 | 0.082 | 0.077 | 0.075 | 0.074 | 0.071 | 0.186 | 0.227 | 0.248 | 0.265 |
请根据表中数据分析同周期元素原子半径的递变规律是______,同主族元素原子半径的递变规律是_____根据表中得出的规律比较Ca2+和Cl-的半径大小:r(Ca2+)_____r(Cl-)(填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有甲、乙、丙三种溶液,进行如下操作:

则甲、乙、丙三种溶液中加的溶质可能是( )
A.BaCl2、H2SO4、KClB.CaCl2、HNO3、AgNO3
C.CaCl2、HNO3、NaClD.BaCl2、HCl、Na2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体血液内的血红蛋白(Hb)易与O2结合生成HbO2,因此具有输氧能力,CO吸入肺中发生反应:CO+HbO2![]() O2+HbCO,37 ℃时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。据此,下列结论错误的是( )
O2+HbCO,37 ℃时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。据此,下列结论错误的是( )
A. 当吸入的CO与O2浓度之比大于或等于0.02时,人的智力才会受损
B. 人体吸入的CO越多,与血红蛋白结合的O2越少
C. CO与HbO2反应的平衡常数K=![]()
D. 把CO中毒的病人放入高压氧仓中解毒,其原理是使上述平衡向左移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2+Ca(OH)2=CaCO3↓+H2O,CaCO3+CO2+H2O=Ca(HCO3)2,且Ca(HCO3)2易溶于水。现有Ca(OH)2溶液,向其溶液中逐渐通入CO2。则下列四个图中,能比较准确地反映出溶液的导电能力和通入CO2气体量的关系的是(x轴表示CO2通入的量,y轴表示导电能力)
A.  B.
B. 
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生兴趣小组模拟工业制取无水Na2SO3的过程如下:

已知:①反应Ⅰ在三颈烧瓶中发生,装置如图所示(固定及加热类仪器省略);
②H2SO3、HSO3-、SO32-在水溶液中的物质的量分数随pH的分布如图;
③Na2SO3·7H2O 和Na2SO3的溶解度曲线如图。
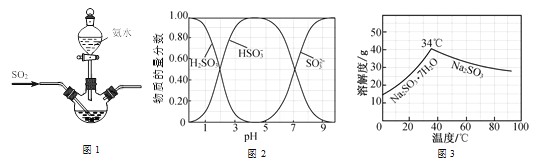
(1)为提高Na2SO3产率,反应Ⅰ应控制pH在_____左右。
(2)反应Ⅱ所得滤液的主要成分是_____和Na2SO3。
(3)将操作Ⅰ后所得的Na2SO3溶液_____(填操作),过滤出的固体用无水乙醇洗涤、在真空干燥箱中采用150℃干燥,得无水Na2SO3固体。
(4)可以用KIO3测定产品中无水Na2SO3的纯度:称取0.1260 g样品于锥形瓶中,用蒸馏水溶解,并加入淀粉做指示剂,滴加酸性KIO3溶液(a mol·L-1)至Na2SO3恰好完全氧化成Na2SO4,发生反应3Na2SO3 + KIO3 = 3Na2SO4 + KI,消耗KIO3溶液体积为b mL。通过计算确定样品中Na2SO3的质量分数(写出计算过程)____
(5)滴加酸性KIO3溶液时,剧烈震荡锥形瓶或者滴加时间过长都会造成所测Na2SO3纯度偏低,原因是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家屠呦呦成功提取到一种分子式为C15H22O5的无色结晶体,命名为青蒿素,这是一种可用于治疗疟疾的固态有机药物,在水溶液中不电离,关于青蒿素的说法正确的是( )
A.5.64g青蒿素含氧原子数目为0.02NA
B.标准状况下2mol青蒿素的体积为44.8L
C.青蒿素属于非电解质
D.青蒿素的摩尔质量为282
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为CaF2、H3BO3(层状结构,层内的H3BO3分子通过氢键结合)、金属铜三种晶体的结构示意图,请回答下列问题:


图Ⅲ 铜晶体中铜原子堆积模型
(1)图Ⅰ所示的CaF2晶体中与Ca2+最近且等距离的F-数为________________,图Ⅲ中未标号的铜原子形成晶体后周围最紧邻的铜原子数为__________________________________。
(2)图Ⅱ所示的物质结构中最外能层已达8电子结构的原子是________,H3BO3晶体中B原子个数与极性键个数比为____________。
(3)金属铜具有很好的延展性、导电性、传热性,对此现象最简单的解释是用________理论。
(4)三种晶体中熔点最低的是________(填化学式),其晶体受热熔化时,克服的微粒之间的相互作用为____________________________________________________________。
(5)已知两个距离最近的Ca2+核间距离为a×10-8cm,结合CaF2晶体的晶胞示意图,CaF2晶体的密度为_______________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com