

 .
. 分析 (1)根据信息淀粉水解生成葡萄糖结合质量守恒书写化学方程式;
(2)根据信息1mol葡萄糖$→_{(发酵)}^{催化剂}$2mol乳酸,转化过程中无其它反应物、生成物结合质量守恒书写化学式;
(3)根据n=$\frac{m}{M}$计算出1.8g乳酸的物质的量,能与过量的饱和NaHCO3溶液反应,说明1个乳酸分子中含有含有一个羧基,另取1.8g乳酸与过量的金属钠反应,测得生成的气体体积为448mL(气体体积已换算为标准状况下体积),则乳酸分子中另一个官能团是醇羟基,据此解答;
(4)经现代化学仪器分析,测定乳酸分子中含有一个甲基,说明醇羟基位于中间碳原子上,根据酯化反应的原理书写六元环状化合物;
解答 解:(1)淀粉水解生成葡糖糖,化学方程式为:(C6H10O5)n+n H2O$\stackrel{催化剂}{→}$n C6H12O6,
故答案为:(C6H10O5)n+n H2O$\stackrel{催化剂}{→}$n C6H12O6;
(2)1mol葡萄糖$→_{(发酵)}^{催化剂}$2mol乳酸,转化过程中无其它反应物、生成物,1mol葡萄糖C6H12O6,含6molC,12molH,6molO,转化为2mol乳酸,所以1mol乳酸中含3molC,6molH,3molO,则乳酸的分子式为C3H6O3;
故答案为:C3H6O3;
(3)1.8g乳酸的物质的量n=$\frac{1.8g}{90g/mol}$=0.02mol,取1.8g乳酸与过量的饱和NaHCO3溶液反应,测得生成的气体体积为448mL(气体体积已换算为标准状况下体积);说明乳酸分子中含有含有羧基,反应生成的二氧化碳气体的物质的量n=$\frac{0.448L}{22.4L/mol}$=0.02mol,说明1个乳酸分子中含有含有一个羧基;另取1.8g乳酸与过量的金属钠反应,测得生成的气体体积为448mL(气体体积已换算为标准状况下体积)生成氢气的物质的量n=$\frac{0.448L}{22.4L/mol}$=0.02mol,1个乳酸分子中含有含有一个羧基,0.02mol乳酸含有0.02mol羧基与金属钠反应生成0.01mol氢气,则乳酸分子中另一个官能团是醇羟基,0.02mol乳酸含有0.02mol醇羟基,与金属钠反应生成0.01mol氢气,乳酸的结构简式可能为 CH3CH(OH)COOH、CH2(OH)CH2COOH;
故答案为:羟基、羧基;CH3CH(OH)COOH、CH2(OH)CH2COOH;
(4)乳酸的结构简式可能为 CH3CH(OH)COOH、CH2(OH)CH2COOH,经现代化学仪器分析,测定乳酸分子中含有一个甲基,说明醇羟基位于中间碳原子上,乳酸的结构简式为CH3CH(OH)COOH,2个乳酸分子在一定条件下可发生酯化反应生成六元环状化合物,反应方程式为:2CH3CH(OH)COOH$→_{加热}^{催化剂}$ +2H2O;
+2H2O;
故答案为: .
.
点评 本题主要考查了乳酸的结构的推导,掌握有机物官能团的性质是解答本题的关键,题目难度中等.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 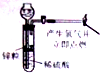 制备并检验氢气的可燃性 | B. | 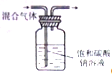 除去CO2中的HCl | ||
| C. | 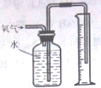 测量O2的体积 | D. | 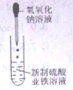 制备氢氧化亚铁并观察其颜色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com