
| A. | 简单离子半径的大小顺序:rX>rY>rZ>rW | |
| B. | 元素Q和Z能形成QZ2型的共价化合物 | |
| C. | Z元素氢化物的沸点高于W元素氢化物的沸点 | |
| D. | X、Y、Z最高价氧化物的水化物之间两两不能发生反应 |
分析 Q、W、X、Y、Z是原子序数依次增大的短周期元素,X的焰色反应呈黄色,则X为Na元素;Q元素的原子最外层电子数是其内层电子数的2倍,Q元素原子有2个电子层,最外层电子数为4,故Q为碳元素;W、Z最外层电子数相同,二者处于同一主族,Z的核电荷数是W的2倍,故Z为硫元素,W为氧元素;元素Y的合金是日常生活中使用最广泛的金属材料之一,则Y为Al元素,以此解答该题.
解答 解:由以上分析可知Q为C元素,W为O元素,X为Na元素,Y为Al元素,Z为S元素,
A.电子层结构相同的离子,核电荷数越大离子半径越小,离子电子层越多离子半径越大,故离子半径Z(S2-)>W(O2-)>X(Na+)>W(Al3+),故A错误;
B.CS2属于共价化合物,故B正确;
C.水分子之间存在氢键,沸点高于硫化氢,故C错误;
D.氢氧化铝是两性氢氧化物,溶于强碱,与氢氧化钠反应生成偏铝酸钠与水,则X、Y、Z最高价氧化物的水化物之间两两能发生反应,故D错误.
故选B.
点评 本题考查位置、结构、性质的关系及应用,为高频考点,侧重考查学生的分析能力,元素的推断是解答本题的关键,并熟悉元素化合物的性质、物质的组成和结构等知识来解答,综合性较强,题目难度中等.


 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源: 题型:选择题
| A. | 含1molFeCl3的饱和溶液滴入沸水中得到胶体数目为NA | |
| B. | 在标准状况下,22.4LCl2和HCl的混合气体中含有的分子总数为2×6.02×1023 | |
| C. | 常温常压下,7.8gNa2S固体和7.8gNa2O2固体中含有的阴离子数目均为0.1NA | |
| D. | 标准状况下,Na2O2与足量的CO2反应生成2.24LO2,转移电子数为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
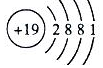

 、
、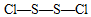 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验 | 现象 | 结论 |
| A | 向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2浊液,加热至沸腾 | 没有砖红色沉淀出现 | 淀粉没有水解成葡萄糖 |
| B | 向某溶液中滴加BaCl2溶液,随后加稀硝酸酸化 | 溶液中产生白色沉淀,加稀硝酸不溶解 | 原溶液中一定含Ag+ |
| C | 将稀硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中 | 溶液变黄色 | 氧化性:H2O2比Fe3+强 |
| D | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体 | 溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
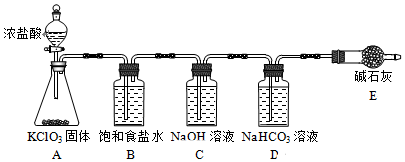
| 实验步骤 | 实验现象 | ||
| B瓶 | C瓶 | D瓶 | |
| 实验1:取样,滴加紫色石蕊溶液 | 变红,不褪色 | 变蓝,不褪色 | 立即褪色 |
| 实验2:取样,测定溶液的pH | 3 | 12 | 7 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
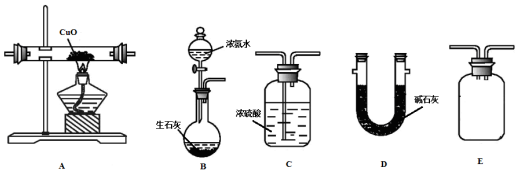
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素 | I1 | I2 | I3 | I4 |
| X | 500 | 4600 | 6900 | 9500 |
| Y | 580 | 1800 | 2700 | 11600 |
| A. | 元素X的常见化合价是+1价 | |
| B. | 若元素Y处于第3周期,它可与冷水剧烈反应 | |
| C. | 元素X与氯形成化合物时,化学式可能是XCl | |
| D. | 元素Y是ⅢA族的元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca2+,Na+,NO3-,Cl- | B. | K+,Ba2+,Cl-,NO3- | ||
| C. | Na+,HCO3-,CO32-,K+ | D. | Na+,Cl-,K+,MnO4- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com