
| A. | NaHSO3溶于水呈酸性:NaHSO3═Na++H++SO32- | |
| B. | 在Na2S2O3溶液中滴加稀硫酸:2H++S2O32-═SO2↑+S↓+H2O | |
| C. | 浓盐酸与MnO2反应制氯气:MnO2+4HCl═Mn2++2Cl2+2H2O | |
| D. | 工业冶炼Mg:2Mg2++2O2-$\frac{\underline{\;电解\;}}{\;}$2Mg+O2↑ |
分析 A.亚硫酸氢根离子部分电离,导致亚硫酸氢钠溶液呈酸性;
B.酸性条件下Na2S2O3与氢离子反应生成二氧化硫、硫单质和水;
C.浓盐酸中的氯化氢应该拆开;
D.该反应不是发生在溶液中,无法书写离子方程式.
解答 解:A.亚硫酸氢根离子的电离方程式应该用可逆号,正确的电离方程式为:HSO3-?H++SO32-,故A错误;
B.在Na2S2O3溶液中滴加稀硫酸,反应生成二氧化硫气体、硫单质和水,反应的离子方程式为:2H++S2O32-═SO2↑+S↓+H2O,故B正确;
C.浓盐酸与MnO2加热制氯气,正确的离子方程式为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,故C错误;
D.工业通过电解熔融氧化镁冶炼,反应的化学方程式为:2MgO(熔融)$\frac{\underline{\;电解\;}}{\;}$2Mg+O2↑,该反应无法改成离子方程式,故D错误;
故选B.
点评 本题考查了离子方程式的书写判断,题目难度不大,注意明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 铜版画的一种制版方法.以沥青涂于薄铜板表面作防腐膜,用刀刻去防腐膜作画,然后放在FeCl3腐蚀液中.刮去膜之处被腐蚀,形成凹线.印刷时凹线可储油墨,在铜版机纸压制下油墨吸于纸上,形成典雅、庄重的铜版画.
铜版画的一种制版方法.以沥青涂于薄铜板表面作防腐膜,用刀刻去防腐膜作画,然后放在FeCl3腐蚀液中.刮去膜之处被腐蚀,形成凹线.印刷时凹线可储油墨,在铜版机纸压制下油墨吸于纸上,形成典雅、庄重的铜版画.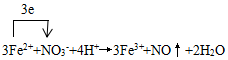 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
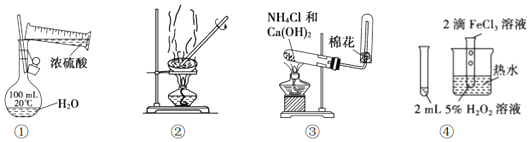
| A. | 用装置①配制一定浓度的硫酸溶液 | |
| B. | 用装置②分离溶解在CCl4中的 I2 | |
| C. | 用装置③制备和收集少量 NH3 | |
| D. | 用装置④验证FeCl3对 H2O2分解有催化作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeSO4溶液存放在加有少量铁粉的试剂瓶中 | |
| B. | 将1mol/L的NaCl溶液保存在容量瓶中 | |
| C. | 凡是给玻璃仪器加热,都要垫石棉网,以防仪器炸裂 | |
| D. | 用pH试纸检验某溶液的酸碱性时,一定要先用蒸馏水湿润 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属性:Na>Mg | B. | 酸性:H2SO4>H2SiO3 | ||
| C. | 稳定性:HCl>HBr | D. | 同浓度溶液的碱性:Na2CO3>NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

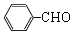 +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2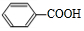 .
. +
+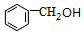 $?_{△}^{浓硫酸}$
$?_{△}^{浓硫酸}$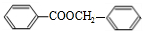 +H2O.
+H2O.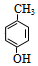 .
.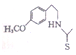 也能发生类似反应④的环化反应,VII的环化产物的结构简式
也能发生类似反应④的环化反应,VII的环化产物的结构简式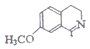 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com