
| A. | ①②③是化学性质不同的粒子 | B. | ①不是核素,②③才是核素 | ||
| C. | ①②③具有相同的质量数 | D. | ①②③互为同位素 |
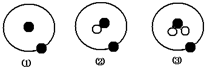
分析 从图示知①、②、③中的质子数等于电子数且都等于1,中子数分别为0、1、2;可知①②③代表的微粒分别为11H、12H、13H,
A.电子数决定化学性质,电子数=质子数;
B.核素是指具有一定数目质子和一定数目中子的一种原子;
C.元素左上角数字表示质量数;
D.质子数相同中子数不同的同种元素的不同原子之间互为同位素.
解答 解:从图示知①、②、③中的质子数等于电子数且都等于1,中子数分别为0、1、2;可知①②③代表的微粒分别为11H、12H、13H,
A.电子数决定化学性质,电子数=质子数,三种原子的电子数相同,化学性质相同,故A错误;
B.①②③代表的微粒分别为11H、12H、13H,都为氢元素的核素,故B错误;
C.11H、12H、13H质量数分别为1、2、3,故C错误;
D.可知①②③代表的微粒分别为11H、12H、13H,质子数相同中子数不同,互为同位素,故D正确;
故选D.
点评 本题考查同位素、核素的概念,题目难度不大.对于元素、核素、同位素、同素异形体、同分异构体、同系物、同种物质等概念的区别是考试的热点问题.


 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应为吸热反应 | B. | CO2的分子模型示意图: | ||
| C. | HCHO分子中既含σ键又含π键 | D. | 每生成1.8 g H2O消耗2.24 L O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H1,△H2都不变 | B. | △H1,△H2都增大 | C. | △H1,△H2都减小 | D. | 不能确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等于90% | B. | 大于90% | C. | 小于90% | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
| 能量(kJ) | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn是正极,Ag2O是负极 | |
| B. | 工作时电子由Zn极经溶液移向Ag2O极 | |
| C. | 该电池可将化学能100%转化为电能 | |
| D. | Zn是负极,反应为Zn-2 e-+2OH-=Zn(OH)2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com