
 ;
; ;
; ;
; ;
;
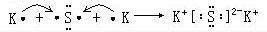 .
. 分析 (1)氮气中存在3对共用电子对,氮原子最外层达到8个电子;
(2)氢氧化钠为离子化合物,电子式中需要标出阴阳离子所带电荷,氢氧根离子需要标出最外层电子;
(3)过氧化钠为离子化合物,由2个钠离子和1个过氧根构成;
(4)二氧化碳中存在两个碳氧键,C、O原子最外层都达到最外层8个电子;
(5)MgCl2属于离子化合物,Mg最外层两个电子被两个Cl原子得到;
(6)K2S为离子化合物,离子化合物阴离子带电荷且用“[]”,共价化合物不带电荷,注意各原子或离子满足稳定结构.
解答 解:(1)氮气中存在氮氮三键,氮气的电子式为 ,
,
故答案为: ;
;
(2)氢氧化钠属于离子化合物,电子式中需要标出阴阳离子所带电荷,钠离子直接用离子符号表示,氢氧根离子需要标出最外层电子,氢氧化钠的电子式为: ,故答案为:
,故答案为: ;
;
(3)Na2O2是钠离子和过氧根离子构成的离子化合物,钠离子失电子形成阳离子,过氧根离子得到电子形成阴离子,电子式为 ,
,
故答案为: ;
;
(4)二氧化碳中存在两对碳氧共用电子对,二氧化碳的电子式为 ,
,
故答案为 ;
;
(5)MgCl2属于离子化合物,Mg最外层两个电子被两个Cl原子得到,用电子式表示形成过程为: ,
,
故答案为: .
.
(6)K2S为离子化合物,用电子式表示形成过程为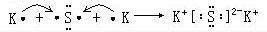 ,
,
故答案为: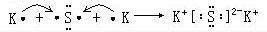 .
.
点评 本题考查用电子式表示离子化合物的形成过程和电子式的书写,难度不大,应先判断化合物种类.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①→④→③→② | B. | ①→③→②→④ | C. | ①→②→③→④ | D. | ①→③→④→② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  4NH3(g)+5O2(g)?4NO+6H2O(g);△H=-Q1kJ/mol(Q1>0) | |
| B. | 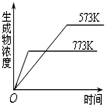 2SO3(g)?2SO2(g)+O2(g);△H=+Q2 kJ/mol(Q2>0) | |
| C. |  N2(g)+3H2(g)?2NH3(g);△H=-Q3kJ/mol(Q3>0) | |
| D. |  H2(g)+CO(g)?C(s)+H2O(g);△H=+Q4kJ/mol(Q4>0) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com