
| A. | Na、Mg、Al的还原性逐渐减弱 | |
| B. | HCl、H2S、PH3、气态氢化物的稳定性逐渐增强 | |
| C. | NaOH、KOH的碱性逐渐增强 | |
| D. | O的原子半径比S的原子半径大 |
分析 A.同周期从左向右金属性减弱;
B.非金属性越强,对应氢化物越稳定;
C.金属性越强,对应碱的碱性越强;
D.同主族从上到下原子半径增大.
解答 解:A.同周期从左向右金属性减弱,则Na、Mg、Al的还原性逐渐减弱,故A正确;
B.非金属性越强,对应氢化物越稳定,则HCl、H2S、PH3的气态氢化物的稳定性逐渐减弱,故B错误;
C.金属性越强,对应碱的碱性越强,则NaOH、KOH的碱性逐渐增强,故C正确;
D.同主族从上到下原子半径增大,则O的原子半径比S的原子半径小,故D错误;
故选BD.
点评 本题考查元素周期律和周期表,为高频考点,把握元素的位置、性质、元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 周期 主族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
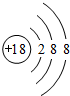 .
.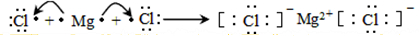 .
. ,该化合物分子内含有极性键(填“极性”或“非极性”).
,该化合物分子内含有极性键(填“极性”或“非极性”).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑥ | B. | ②③⑤⑥ | C. | ②③④⑤ | D. | ①③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化铁和稀硫酸反应:Fe2O3+6H+=2Fe2++3H2O | |
| B. | 碳酸氢钠溶液中加稀硫酸:CO32-+2H+=H2O+CO2↑ | |
| C. | 氢氧化钡溶液加入稀硫酸中:OH-+H+ H2O | |
| D. | Cu(OH)2加入H2SO4:2H++Cu(OH)2=Cu2++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com