
【题目】25℃时,下列有关溶液中粒子的物质的量浓度关系正确的是( )
A. 0.1mol/|LCH3COONa 与0.lmol/LHCl 溶液等体积混合: c(Na+)=c(Cl-)>c(OH-)>cCH3COO-)
B. 0.lmol/LNH4Cl与0.lmol/L 氨水等体积浪合(pH>7): c(NH3·H2O)>c(NH4+)>c(Cl-)>c(OH-)
C. 0.1mol/LNa2CO3与0.lmol/LNaHCO3溶液等体积混合:2/3c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)
D. 0.1mol/LNa2C2O4与0.lmol/LHCl溶液等体积混合(H2C2O4为二元弱酸):2c(C2O42-)+c(HC2O4-)+c(OH-)=c(Na+)+c(H+)
【答案】C
【解析】A.溶液为氯化钠和醋酸混合溶液,且二者的物质的量浓度相等,混合溶液呈酸性,溶液中c(OH-)很小,且混合溶液中存在物料守恒,根据物料守恒得c(Na+)=c(Cl-),醋酸部分电离,由于氢离子来自水的电离和醋酸的电离,则c(H+)>c(CH3COO-),溶液中正确的离子浓度大小为:c(Na+)=c(Cl-)>c(H+)>c(CH3COO-),故A错误;B.混合溶液呈碱性,说明NH3H2O的电离程度大于NH4+的水解程度,则溶液中c(NH3H2O)<c(NH4+),故B错误;C.混合溶液存在物料守恒,根据物料守恒得:0.1molL-1Na2CO3溶液中:c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3),0.1molL-1NaHCO3溶液中:c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3),两式相加得:2c(Na+)=3c(CO32-)+3c(HCO3-)+3c(H2CO3),即 ![]() c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3),故C正确;D.任何电解质溶液中都存在电荷守恒,根据电荷守恒得2c(C2O42-)+c(HC2O4-)+c(OH-)+c(Cl-)=c(Na+)+c(H+),故D错误;故选C。
c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3),故C正确;D.任何电解质溶液中都存在电荷守恒,根据电荷守恒得2c(C2O42-)+c(HC2O4-)+c(OH-)+c(Cl-)=c(Na+)+c(H+),故D错误;故选C。


科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是短周期中的常见元素,其部分性质如下表,下列说法不正确的是( )
W | 单质是淡黄色固体 |
X | 第三周期原子半径最小的金属 |
Y | 单质不能将比它不活泼的金属从盐溶液中置换出来 |
Z | 原子最外层电子数是电子总数的 |
A.Y、X、W的原子半径依次减小,X、Y、W单核离子的半径依次增大
B.W、X、Y的最高价氧化物的水化物之间可以两两反应
C.Y的氧化物与Z的最高价氧化物反应一定是氧化还原反应
D.W、Z、X、Y的最高正价依次降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实现 “节能减排” 和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源。目前工业上有一种方法是用CO2来生产燃料甲醇。一定条件下发生反应:
CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g),下图1表示该反应过程中能量(单位为kJ·mol-1)的变化:
CH3OH(g)+H2O(g),下图1表示该反应过程中能量(单位为kJ·mol-1)的变化:
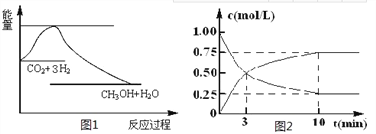
(1)关于该反应的下列说法中,正确的是____________(填字母)。
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
(2)为探究反应原理,现进行如下实验,在体积为l L的密闭容器中,充入l mol CO2和4mol H2,一定条件下发生反应:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如上图2所示。
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如上图2所示。
①从反应开始到平衡,CO2的平均反应速率v(CO2)=_________;
②下列措施中能使化学平衡向正反应方向移动的是___________(填字母)。
A.升高温度B.将CH3OH(g)及时液化抽出C.选择高效催化剂D.再充入l molCO2和4 molH2
(3)25℃,1.01×105Pa时,16g 液态甲醇完全燃烧,当恢复到原状态时,放出363.3kJ的热量,写出该反应的热化学方程式:_____________。
(4)选用合适的合金为电极,以氢氧化钠、甲醇、水、氧气为原料,可以制成一种以甲醇为原料的燃料电池,此电池的负极的电极反应式是:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
①原子中处于第3能层的电子跃迁到第2能层时需要放出能量;②M能层可以有s、p、d、f能级;
③3p正表示有3个p正轨道;④在一个原子中,不可能出现运动状态完全相同的两个电子;⑤2s电子云有两个空间取向。
A. ①②③ B. ①④ C. ②⑤ D. ③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】250℃和1.01×105Pa时,反应 2N2O5(g)=4NO2(g)+O2(g) △H=+56.76kJ/mol,自发进行的原因( )
A. 是吸热反应 B. 是放热反应
C. 是熵减少的反应 D. 熵增大效应大于焓增大的效应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去硫酸铜溶液中含有的Fe2+杂质,先加入合适的氧化剂使Fe2+氧化为Fe3+,下列物质中最好选用
A. Cl2水 B. H2O2溶液 C. KMnO4溶液 D. HNO3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com