
| A. | a与其他元素生成的化合物都是离子化合物 | |
| B. | b与氢形成的所有化合物中化学键均为极性共价键 | |
| C. | c存在两种或两种以上的氧化物 | |
| D. | 在四种元素中,d元素的非金属性最强 |
分析 a.b.c.d为短周期元素,a的M电子层有1个电子,所以a的电子数为11,则a为Na元素;b原子最外层电子数为最内层电子数的2倍,其最外层电子数是4,为C元素;
c元素的最高化合价为最低化合价绝对值的3倍,则c为S元素;c与d同周期,d的原子半径小于c,则d为Cl元素;结合元素化合物的性质与元素周期律解答.
解答 解:a.b.c.d为短周期元素,a的M电子层有1个电子,所以a的电子数为11,则a为Na元素;b原子最外层电子数为最内层电子数的2倍,其最外层电子数是4,为C元素;c元素的最高化合价为最低化合价绝对值的3倍,则c为S元素;c与d同周期,d的原子半径小于c,则d为Cl元素,
A.a为Na元素,是活泼的金属元素,与其他非金属元素形成离子化合物,故A正确;
B.a为Na元素,是活泼的金属元素,与H元素形成NaH为离子化合物,只有离子键,没有共价键,故B错误;
C.Na、C、S、Cl均存在两种或两种以上的氧化物,故C正确;
D.四种元素中非金属性最强的是Cl(d),故D正确;
故选B.
点评 本题考查原子结构和元素周期律的关系,题目难度中等,涉及元素推断、元素周期律、化学键等知识点,侧重考查学生分析判断及知识运用能力,明确原子结构与元素周期律、元素周期表的关系为解答关键.


 名校通行证有效作业系列答案
名校通行证有效作业系列答案科目:高中化学 来源: 题型:选择题
| A. | 将苯和溴水混合后加入铁粉制取湨苯 | |
| B. | 检验溴乙烷中的湨元素的方法是加入NaOH溶液共热,冷却后滴入AgNO3溶液,观察有无浅黄色沉淀生成 | |
| C. | 将硝酸银溶液加入到浓氨水中配成银氨溶液后,滴加几滴乙醛加热煮沸制银镜 | |
| D. | 蒸馏操作中,将温度计放置在蒸馏烧瓶支管口附近 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 原因 | 结论 |
| A | 乙烯和苯都能使溴水褪色 | 苯和乙烯分子都含有碳碳双键 |
| B | 乙酸乙酯和乙烯一定条件下都能和水反应 | 两者属于同一类型的反应 |
| C | 乙酸和葡萄糖都能与新制的氢氧化铜悬浊液反应 | 两者所含的官能团相同 |
| D | 乙烯能使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色 | 两者褪色的本质不相同 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
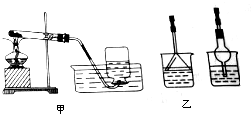 在实验室里用KClO3和MnO2的混合物加热制取少量的氧气,装置如图甲.实验结束后要先取出导气管,后撤走酒精灯,以防止水倒吸回试管的受热部分,引起试管的破裂.
在实验室里用KClO3和MnO2的混合物加热制取少量的氧气,装置如图甲.实验结束后要先取出导气管,后撤走酒精灯,以防止水倒吸回试管的受热部分,引起试管的破裂.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在合成氨工业中,移走NH3可增大正反应速率,提高原料转化率 | |
| B. | 锅炉中沉积的CaSO4可用饱和碳酸钠溶液浸泡,再用盐酸溶解而除去 | |
| C. | 将AlCl3溶液蒸干、灼烧至恒重,最终剩余固体是AlCl3 | |
| D. | 加热Fe2(SO4)3溶液,Fe3+的水解程度和溶液的pH均增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 最外层电子数大于4的一定是非金属元素 | |
| B. | 元素周期表有18纵列,7横行,故有18个族,7个周期 | |
| C. | 第ⅠA族就是碱金属 | |
| D. | 某ⅡA族元素的原子序数为a,则和其同周期ⅢA的元素的原子序数可能为a+11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑥ | B. | ③④⑤⑥ | C. | ①③⑥ | D. | ③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com