
某中学化学兴趣小组为了调查当地某一湖泊的水质污染情况,在注入湖泊的3 个主要水源的入口处采集水样,并进行了分析,给出了如下实验信息:其中一处水源含有A、B两种物质,一处含有C、D两种物质,一处含有E物质,A、B、C、D、E为五种常见化合物,均由下表中的离子形成:
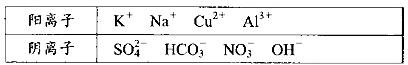
为了鉴别上述化台物。分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B、c为紫色(透过蓝色钻玻璃);
④在各溶液中加入硝酸锁溶液,再加过量稀硝酸,A中放出无色气体,C、D中都能产
生白色沉淀:
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)写出B、D的化学式:B________,D________。
(2)将含I mol A的溶液与含l molE的溶液反应后蒸于,仅得到一种化台物,该化合物的化学式为_____________.
(3)在A溶液中加入少量澄清石灰水,其离子方程式为________________。
(4)C常用作净水剂,用离子方程式和适当文字说明其净水原理_____________。
(5)若向含溶质lmol的C溶液中逐滴加入Ba(OH)2溶液,生成沉淀质量最大为______________g。
【知识点】离子反应C5D5B1
【答案解析】(1)KNO3(2分) CuSO4(2分) (2)Na2CO3(2分)
(3)2HCO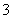 + Ca2+ +2OH- = CaCO3↓ + CO
+ Ca2+ +2OH- = CaCO3↓ + CO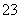 + H2O(2分)
+ H2O(2分)
(4)Al3+ + 3H2O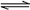 Al(OH)3(胶体)+3H+水解生成的氢氧化铝胶体能吸附水中的悬浮物净水(2分)
Al(OH)3(胶体)+3H+水解生成的氢氧化铝胶体能吸附水中的悬浮物净水(2分)
(5)466(2分)
解析:根据D为蓝色溶液知其含Cu2+,根据②的信息知E含OH-,C含Al3+,根据③知B、c含K+,根据④知A含HCO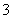 ,C、D含Ba2+,则B为KNO3,D为CuSO4,E为氢氧化钠(OH-只能与K+或Na+结合,A、E中没有K+),A为碳酸氢钠, C为硫酸钾铝。A溶液中加入少量澄清石灰水,则OH-反应完,即2HCO
,C、D含Ba2+,则B为KNO3,D为CuSO4,E为氢氧化钠(OH-只能与K+或Na+结合,A、E中没有K+),A为碳酸氢钠, C为硫酸钾铝。A溶液中加入少量澄清石灰水,则OH-反应完,即2HCO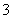 + Ca2+ +2OH- = CaCO3↓ + CO
+ Ca2+ +2OH- = CaCO3↓ + CO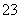 + H2O,向硫酸钾铝溶液中逐滴加入Ba(OH)2溶液,若生成沉淀的物质的量最大,反应是2KAl(SO4)+3Ba(OH)2=3BaSO4↓+Al(OH)3↓+K2SO4,生成沉淀质量最大时,SO42-继续沉淀,Al(OH)3变为偏铝酸根离子,即生成2mol硫酸钡,为466g。
+ H2O,向硫酸钾铝溶液中逐滴加入Ba(OH)2溶液,若生成沉淀的物质的量最大,反应是2KAl(SO4)+3Ba(OH)2=3BaSO4↓+Al(OH)3↓+K2SO4,生成沉淀质量最大时,SO42-继续沉淀,Al(OH)3变为偏铝酸根离子,即生成2mol硫酸钡,为466g。
【思路点拨】获取题目中的信息是解题的关键,另外可根据离子共存进行离子组合,解答⑸时需注意“生成沉淀质量最大时”。


科目:高中化学 来源: 题型:
某有机物其结构简式为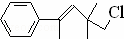 ,关于该有机物下列叙述正确的是( )
,关于该有机物下列叙述正确的是( )
|
| A. | 不能使酸性KMnO4溶液褪色 |
|
| B. | 能使溴水褪色 |
|
| C. | 在加热和催化剂作用下,最多能和4 mol H2反应 |
|
| D. | 一定条件下,能和NaOH醇溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
工厂排放的SO2烟气对环境造成污染,某企业用下列流程综合处理,下列有关说法正确的是( )
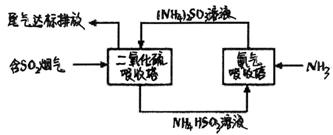
A.二氧化硫吸收塔中发生的反应为:SO2+ SO32-+H2O=2HSO3-
B.氨气吸收塔中发生的反应为:HSO3-+OH-= H2O+ SO32-
C.上述流程利用的是氧化还原反应原理
D.上述流程可循环利用的物质有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系:
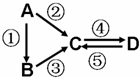
(1)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。B与C在一定条件下反应生成的A是大气的主要成分,写出该反应的化学方程式:______________________________。
(2)若D物质具有两性,②、③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体。判断单质A的元素在周期表中的位置:__________________。
(3)若A是太阳能电池用的光伏材料。C、D为钠盐,两种物质中钠、氧外的元素为同一主族,且溶液均显碱性。写出②反应的化学方程式:__________________________________。
(4)若A是应用最广泛的金属。④反应用到A,②、⑤反应均用到同一种非金属单质。C的溶液用于蚀刻印刷铜电路板,写出该反应的离子方程式:__________________________。
(5)若A为淡黄色固体,C、D是氧化物,且C是造成酸雨的主要物质. B与C可反应生成A。请写出B的电子式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学在生产和生活中有着重要的应用,下列说法正确的是( )
A.“雾霾天气”、“温室效应”、“光化学烟雾”的形成都与氮氧化物有关
B.“辽宁舰”上用于舰载机降落拦阻索的特种钢缆,属于新型无机非金属材料
C.白酒中混有少量塑化剂,少量饮用对人体无害,可通过过滤方法除去
D.能够改善食品的色、香、味,并有防腐、保鲜作用的食品添加剂,须限量使用
查看答案和解析>>
科目:高中化学 来源: 题型:
.水溶液X中只可能溶有K+、Mg2+、Al3+、AlO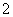 、SiO
、SiO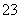 、SO
、SO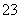 、CO
、CO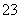 、SO
、SO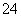 中的若干种离子。某同学对该溶液进行了如图实验:
中的若干种离子。某同学对该溶液进行了如图实验:
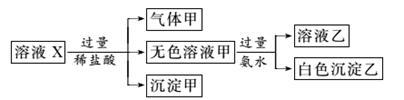
下列判断正确的是( )
A.气体甲一定是纯净物
B.沉淀甲是硅酸和硅酸镁的混合物
C.K+、AlO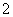 和SiO
和SiO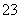 一定存在于溶液X中
一定存在于溶液X中
D.CO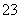 和SO
和SO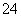 一定不存在于溶液X中
一定不存在于溶液X中
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实不能用化学平衡移动原理解释的是( )
A.光照新制的氯水时,溶液的pH逐渐减小
B.加催化剂,使N2和H2在一定条件下转化为NH3
C.可用浓氨水和氢氧化钠固体快速制取氨气
D.增大压强,有利于SO2与O2反应生成SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
在容积为2 L的密闭容器中充入3mol气体A和2.5mol气体B,发生反应:3A(g)+B(g)xC(g)+2D(g)(正反应为吸热反应),5min时测得生成1mol D,C的平均反应速率v(C)=0.1mol·L-1·min-1,试求:
(1)方程式中C的化学计量数x=__________。
(2)5min内A的平均反应速率v(A)=__________。
(3)5min时B的转化率为__________。
(4)温度升高A的转化率________(填“增大”或“减小”或“不变”下同),压强增大B的转化率________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是()
A. 需要加热才能发生的反应不一定是吸热反应
B. 任何放热反应在常温条件下一定能发生
C. 反应物和生成物所具有的总能量的相对大小决定了反应是放热还是吸热
D. 吸热反应在一定条件下(如常温、加热等)也能发生
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com