
【题目】KClO3和浓盐酸在一定温度下反应会生成红黄色的易爆物二氧化氯。
(1)请完成该过程的化学方程式并配平。
____KClO3+___HCl(浓)===____KCl+____ClO2↑+____Cl2↑+___(_________)
(2)浓盐酸在反应中显示出来的性质是__(填写编号)。
①氧化性 ②还原性 ③酸性 ④碱性
(3)若反应生成0.1molCl2,则转移的电子数为__。
(4)ClO2具有很强的氧化性。因此,常被用作消毒剂,其消毒的效率(以单位质量得到的电子数表示)1kgClO2相当于___kgCl2。(提示:Cl2和ClO2在消毒过程中均变为Cl-)
【答案】2 4 2 2 1 2 H2O ②③ 1.204×1023(或0.2×6.02×1023) 2.63
【解析】
(1)KClO3中氯元素化合价降低1价生成ClO2;两个HCl中氯元素化合价升高2价生成Cl2,化合价升降最小公倍数为2,故ClO2系数乘以2,KClO3系数乘以2,HCl系数先为2,再结合原子守恒配平,最终反应方程式为:2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O;
(2)KClO3是氧化剂,被还原生成ClO2;HCl(浓)是还原剂,被氧化生成Cl2,但是有部分HCl中的Cl的化合价没有变化,生成KCl,体现出酸性,浓盐酸既表现还原性也表现酸性;
(3)根据化学方程式,每生成1molCl2转移2mol电子,现生成0.1 mol Cl2,则转移了0.2mol电子,转移的电子数为1.204×1023(或0.2×6.02×1023);
(4)ClO2![]() Cl-,化合价降低了5价,失去了5个电子;Cl2
Cl-,化合价降低了5价,失去了5个电子;Cl2![]() 2Cl-,化合价共降低2价,得到了2个电子;根据题意,设1kgClO2相当于xkgCl2,有
2Cl-,化合价共降低2价,得到了2个电子;根据题意,设1kgClO2相当于xkgCl2,有![]() ×5=
×5=![]() ×2,得x=2.63。
×2,得x=2.63。


 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】已知:物质的能量越低越稳定,白磷转化为红磷是放热反应,下列说法中正确的是( )
A. 白磷转化为红磷是物理变化
B. 红磷和白磷互为同素异形体
C. 相同条件下,红磷所具有的总能量比白磷的高
D. 在相同条件下白磷比红磷稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸工业的有关叙述错误的是( )
A. 硫铁矿磨成粉末,可加快反应速率
B. 煅烧硫铁矿时鼓入较大量空气,可提高原料利用率
C. 接触室(发生反应:2SO2+O2 ![]() 2SO3)使用热交换器,可充分利用能量
2SO3)使用热交换器,可充分利用能量
D. 接触室出来的气体被浓硫酸(SO3溶于其中)吸收后,可直接排放到空气中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上通过电解精制饱和食盐水来制备NaOH、H2、Cl2,再合成盐酸。完成下列填空:
(1)粗盐提纯:为除去粗盐中的Ca2+、Mg2+、SO42—。向粗盐溶液中依次加入稍过量的NaOH溶液、______,过滤后,再向滤液中加入适量__________,再蒸发。
(2)电解饱和食盐水:25℃,电解10L饱和食盐水,若阴极收集到标准状况下11.2L_______(填气体化学式),则溶液pH=_______(设溶液体积、温度不变、忽略生成物间的反应)。
(3)工业制盐酸:利用Cl2和H2化合,所得产物再溶于水的方法制得盐酸,生产流程如下:
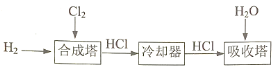
为确保Cl2完全反应,合成塔中n(H2)略大于n(Cl2)。写出一条Cl2必须反应完全的理由:______。
(4)盐酸浓度测定:可用滴定法,用盐酸滴定已知质量Na2CO3的溶液。过程如下:准确称量一定质量的Na2CO3固体于锥形瓶中,加蒸馏水使其溶解,滴加指示剂X,用待测盐酸滴定,接近终点时,加热锥形瓶,煮沸液体2min,冷却至室温,继续滴定至终点,记录消耗盐酸的体积。重复上述过程三次,计算盐酸浓度。
已知:指示剂X的变色范围是5.0~5.2; 25℃,饱和CO2水溶液pH≈4。
①本测定用的仪器有锥形瓶、烧杯、玻璃棒、____________________________________。
②本测定的反应原理是________________________________(用化学方程式表示)。
③接近终点时煮沸反应混合物的目的是_______________________________。
④盛放Na2CO3固体的锥形瓶不干燥,对实验结果的影响是_________(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 代表阿伏伽德罗常数的值,下列有关说法正确的是( )
代表阿伏伽德罗常数的值,下列有关说法正确的是( )
A.常温常压下,2.24 L SO2与O2混合气体中所含氧原子数小于0.2![]()
B.电解饱和食盐水时,当溶液pH由7变为13,电路中转移的电子数为0.1![]()
C.常温下,1 L pH=13的Ba(OH)2中含有的OH- 数目为0.2![]()
D.10 mL 98%的H2SO4溶液,加入水中稀释至100 mL,H2SO4的质量分数为9.8%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食品化学家A.SaariCsallany和Christine Seppanen研究发现,当豆油被加热到油炸温度(185 ℃)时,会产生如下所示高毒性物质,许多疾病和这种有毒物质有关,如帕金森症。下列关于这种有毒物质的判断不正确的是
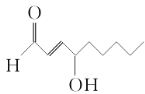
A. 该物质属于烃的衍生物
B. 该物质的分子式为C9H14O2
C. 该物质分子中含有三种官能团
D. 该物质最多可以和2 mol H2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,充分燃烧一定量的丁烷生成二氧化碳和气态水时放出热量Q kJ(Q>0)。经测定完全吸收生成的CO2需消耗5 mol·L-1的KOH溶液100 mL,恰好生成正盐。则此条件下反应C4H10(g)+13/2O2(g)![]() 4CO2(g)+5H2O(g)的ΔH为( ) kJ·mol-1
4CO2(g)+5H2O(g)的ΔH为( ) kJ·mol-1
A. +8Q B. +16Q C. -8Q D. -16Q
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入M的浓溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑两球的浮力变化)
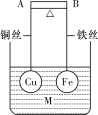
A. 当M为盐酸、杠杆为导体时,A端高,B端低
B. 当M为AgNO3、杠杆为导体时,A端高,B端低
C. 当M为CuSO4、杠杆为导体时,A端低,B端高
D. 当M为CuSO4、杠杆为绝缘体时,A端低,B端高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com