
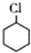
 (一氯环己烷)$→_{II}^{NaOH,乙醇,△}$
(一氯环己烷)$→_{II}^{NaOH,乙醇,△}$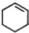 $→_{Ⅲ}^{Br_{2}的CCl_{4}溶液}$B$\stackrel{Ⅳ}{→}$
$→_{Ⅲ}^{Br_{2}的CCl_{4}溶液}$B$\stackrel{Ⅳ}{→}$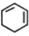

 .
. 分析 A发生取代反应生成一氯环己烷,则A为 ,一氯环己烷发生消去反应生成环己烯,环己烯和溴发生加成反应生成B,B结构简式为
,一氯环己烷发生消去反应生成环己烯,环己烯和溴发生加成反应生成B,B结构简式为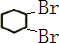 ,B发生消去反应生成
,B发生消去反应生成 ,结合题目分析解答.
,结合题目分析解答.
解答 解:A发生取代反应生成一氯环己烷,则A为 ,一氯环己烷发生消去反应生成环己烯,环己烯和溴发生加成反应生成B,B结构简式为
,一氯环己烷发生消去反应生成环己烯,环己烯和溴发生加成反应生成B,B结构简式为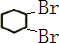 ,B发生消去反应生成
,B发生消去反应生成 ,
,
①通过以上分析知,A的结构简式是 ,I的反应类型是取代反应,II的反应类型消去反应,
,I的反应类型是取代反应,II的反应类型消去反应,
故答案为: ;消去反应;取代反应;
;消去反应;取代反应;
②反应Ⅳ为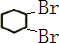 的消去反应,反应的化学方程式为
的消去反应,反应的化学方程式为 ,
,
故答案为: .
.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断能力,明确反应条件与反应类型的关系来推出各物质是解答本题的关键,注意卤代烃的水解、消去反应的条件,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 在5-氨基四唑(
在5-氨基四唑(  )中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊.
)中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 置换反应 | B. | 分解反应 | C. | 化合反应 | D. | 复分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 冰晶石能降低Al2O3的熔点,用Al2O3炼铝时加入它可减少能耗 | |
| B. | Mg在空气中燃烧时发出耀眼的白光,可用于制造信号弹 | |
| C. | 氧化钠能与H2O、CO2反应,可用作漂白剂和供氧剂 | |
| D. | 常温时浓硝酸与铁不反应,可用铁桶贮存浓硝酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | A | B | C | D |
| 实验 方案 | 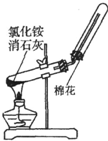 | 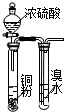 | 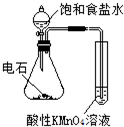 |  置于光亮处 |
| 实验 目的 | 制取并收集氨气 | 验证浓硫酸的强氧化性 | 验证乙炔的还原性 | 验证甲烷与氯气发生 化学反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
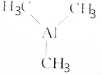 )可用于金属有机化合物气相沉积,下列有关说法正确的是( )
)可用于金属有机化合物气相沉积,下列有关说法正确的是( )| A. | 三甲基铝的摩尔质量是72 | |
| B. | 14.4g三甲基铝中碳原子数为0.6NA | |
| C. | 0.5mol三甲基铝的质量为36g•mol-1 | |
| D. | 1mol三甲基铝在标准状况下的体积约为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com