
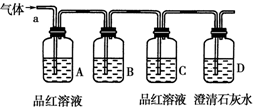
某化学兴趣小组为了探究某些气体的性质,设计了如下图所示的实验装置.实验时将A、D中产生的气体同时通入C中.(K为止水夹,部分夹持仪器已略去)
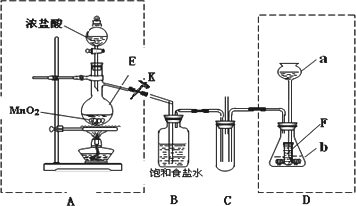
回答下列问题:
(1)简述实验前检查A部分装置的气密性的方法________.
(2)仪器E的名称是________,锥形瓶内小试管F的作用是________.
(3)若b是生石灰、a是________时,在C中有白烟产生,写出生成白烟的总的化学方程式________.
(4)若a是质量分数为75%的硫酸,b是亚硫酸钠粉末,在C中盛适量的BaCl2溶液时,写出C中发生反应的总的离子方程式:________.
(5)若a是饱和食盐水,b是电石,写出D中发生反应的化学方程式:________,该有机产物的名称为________.
(6)从环保的角度出发,上述实验装置中需要改进的是:________.
 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、C(石墨) | 稀盐酸 | 偏向石墨 |
| 4 | Mg、Al | 氢氧化钠溶液 | 偏向Mg |
| 5 | Al、Zn | 浓硝酸 | 偏向Al |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
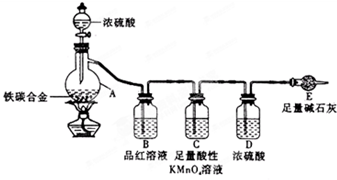 某化学兴趣小组为了测定某铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了如图所示的实验装置和实验方案(夹持仪器已省略),请据此项回答相应问题.
某化学兴趣小组为了测定某铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了如图所示的实验装置和实验方案(夹持仪器已省略),请据此项回答相应问题.| △ |
| ||
| ||
| 3b |
| 11a |
| 3b |
| 11a |
查看答案和解析>>
科目:高中化学 来源: 题型:
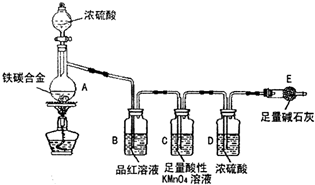 某化学兴趣小组为了测定某铁碳合金(看成铁和碳两种单质的混合物)中铁的质量分数,并探究浓硫酸的某些性质,设计了如图所示的装置(夹持仪器已省略)和方案进行实验.
某化学兴趣小组为了测定某铁碳合金(看成铁和碳两种单质的混合物)中铁的质量分数,并探究浓硫酸的某些性质,设计了如图所示的装置(夹持仪器已省略)和方案进行实验.查看答案和解析>>
科目:高中化学 来源: 题型:
 某化学兴趣小组为了探究常温下某非金属氧化物形成的未知气体的成分.该小组成员将气体通入澄清石灰水,发现澄清石灰水变浑浊,持续通入发现浑浊又变澄清,由此该小组成员对气体的成分提出猜想.
某化学兴趣小组为了探究常温下某非金属氧化物形成的未知气体的成分.该小组成员将气体通入澄清石灰水,发现澄清石灰水变浑浊,持续通入发现浑浊又变澄清,由此该小组成员对气体的成分提出猜想.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com