
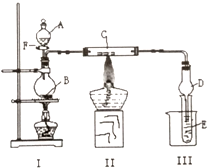
 ÓĆČēĶ¼ĖłŹ¾×°ÖĆ½ųŠŠÓŠ¹ŲŹµŃ飬°Īµō·ÖŅŗĀ©¶·ÉĻæŚ²£Į§Čū£¬“ņæŖF£¬½«AÖšµĪ¼ÓČėÖĮBÖŠ£®
ÓĆČēĶ¼ĖłŹ¾×°ÖĆ½ųŠŠÓŠ¹ŲŹµŃ飬°Īµō·ÖŅŗĀ©¶·ÉĻæŚ²£Į§Čū£¬“ņæŖF£¬½«AÖšµĪ¼ÓČėÖĮBÖŠ£®·ÖĪö £Ø1£©¢ŁAŹĒŹµŃéŹŅµÄŅ»ÖÖ³£ÓĆČ¼ĮĻ£¬ĒŅÄܹ»ÓėCuOŌŚ¼ÓČČĢõ¼žĻĀ·“Ӧɜ³Éŗ¬ÓŠČ©»łµÄĪļÖŹ£¬ŌņAĪŖŅŅ“¼£¬ŅŅ“¼ÖŠŗ¬ÓŠÉŁĮæĖ®·Ö£¬¶ųÓ²ÖŹ¹ÜÖŠŠčŅŖ¼ÓČČ£¬ČŻŅ×µ¼ÖĀÓ²ÖŹ¹ÜÕØĮŃ£¬¾Ż“Ė·ÖĪöŃõ»ÆøʵÄ×÷ÓĆ£»
¢ŚŹŌ¹ÜCÖŠŅŅ“¼ÓėŃõ»ÆĶŌŚ¼ÓČČĢõ¼žĻĀ·¢ÉśŃõ»Æ»¹Ō·“Ӧɜ³ÉŅŅČ©”¢CuŗĶĖ®£»
¢ŪŹŌ¹ÜEÖŠŅŅČ©ÓėŅų°±ČÜŅŗ·“Ӧɜ³É“×Ėįļ§”¢Ņų”¢°±ĘųŗĶĖ®£¬¾Ż“ĖŠ“³ö·“Ó¦µÄ»Æѧ·½³ĢŹ½£»
¢ÜŅĒĘ÷DĪŖĒņŠĪøÉŌļ¹Ü£¬æÉÓŠ·ĄÖ¹µ¹ĪüµÄ×÷ÓĆ£»
£Ø2£©¢ŁAŹĒŅ»ÖÖŗ¬ÓŠČ©»łµÄ±„ŗĶŅ»ŌŖōČĖį£¬ŌņAĪŖHCOOH£¬øł¾ŻĢāÖŠŠÅĻ¢æÉÖŖ£ŗ¼×ĖįŌŚÅØĮņĖį×÷ÓĆĻĀ·Ö½āÉś³ÉCOŗĶĖ®£»
¢ŚĢ¼ĖįµÄĖįŠŌ“óÓŚ±½·Ó£¬Ōņ¶žŃõ»ÆĢ¼Óė±½·ÓÄĘČÜŅŗ·“Ӧɜ³É±½·Ó£¬±½·ÓČܽā¶Č½ĻŠ”£¬ŌņŹŌ¹ÜÖŠ±ä»ė×Ē£»
¢Ū±½·ÓŌŚ·ŠĖ®ÖŠŅ×ČÜ£¬ŌņŹŌ¹ÜÖŠČÜŅŗ±ä³ĪĒ壮
½ā“š ½ā£ŗ£Ø1£©AŹĒŹµŃéŹŅµÄŅ»ÖÖ³£ÓĆČ¼ĮĻ£¬ĒŅÄܹ»ÓėCuOŌŚ¼ÓČČĢõ¼žĻĀ·“Ӧɜ³Éŗ¬ÓŠČ©»łµÄĪļÖŹ£¬ŌņAĪŖŅŅ“¼£¬
¢ŁŅŅ“¼ÖŠ»įŗ¬ÓŠÉŁĮæĖ®·Ö£¬¶ųÓ²ÖŹ¹ÜÖŠŠčŅŖ¼ÓČČ£¬ĪŖĮĖ±ÜĆāŹŌ¹ÜÕØĮŃ£¬ŠčŅŖÓĆŃõ»ÆøĘĪüŹÕŅŅ“¼ÖŠµÄĖ®·Ö£¬
¹Ź“š°øĪŖ£ŗĪüŹÕŅŅ“¼ÖŠŗ¬ÓŠµÄĖ®·Ö£¬·ĄÖ¹Ė®ÕōĘų½ųČėÓ²ÖŹ¹Ü£»
¢ŚŹŌ¹ÜCÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗC2H5OH+CuO$\stackrel{”÷}{”ś}$CH3CHO+Cu+H2O£¬
¹Ź“š°øĪŖ£ŗC2H5OH+CuO$\stackrel{”÷}{”ś}$CH3CHO+Cu+H2O£»
¢ŪŅŅČ©ŌŚĖ®Ō”¼ÓČČĢõ¼žŗĶŅų°±ČÜŅŗ·“Ӧɜ³Éµ„ÖŹŅų£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗCH3CHO+2Ag£ØNH3£©2OH$\stackrel{Ė®Ō”¼ÓČČ}{”ś}$CH3COONH4+2Ag”ż+3NH3+H2O£¬
¹Ź“š°øĪŖ£ŗCH3CHO+2Ag£ØNH3£©2OH$\stackrel{Ė®Ō”¼ÓČČ}{”ś}$CH3COONH4+2Ag”ż+3NH3+H2O£»
¢ÜĒņŠĪøÉŌļ¹ÜæÉŅŌĘšµ½·ĄÖ¹µ¹ĪüµÄ×÷ÓĆ£¬
¹Ź“š°øĪŖ£ŗ·ĄÖ¹µ¹Īü£»
£Ø2£©¢ŁAŹĒŅ»ÖÖŗ¬ÓŠČ©»łµÄ±„ŗĶŅ»ŌŖōČĖį£¬ŌņAĪŖHCOOH£¬øł¾ŻŠÅĻ¢æÉÖŖ£¬¼×ĖįŌŚÅØĮņĖį×÷ÓĆĻĀ·Ö½āÉś³ÉŅ»Ńõ»ÆĢ¼ŗĶĖ®£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗHCOOH$”ś_{”÷}^{ÅØĮņĖį}$CO”ü+H2O£¬
¹Ź“š°øĪŖ£ŗHCOOH$”ś_{”÷}^{ÅØĮņĖį}$CO”ü+H2O£»
¢ŚÓÉÓŚ¶žŃõ»ÆĢ¼Óė±½·ÓÄĘ·“Ӧɜ³É±½·Ó£¬±½·ÓĪ¢ČÜÓŚĖ®£¬ĖłŅŌŹŌ¹ÜÖŠČÜŅŗ±ä»ė×Ē£¬
¹Ź“š°øĪŖ£ŗ¶žŃõ»ÆĢ¼Óė±½·ÓÄĘ·“Ӧɜ³É±½·Ó£¬±½·ÓĪ¢ČÜÓŚĖ®£»
¢Ū±½·ÓŅ×ČÜÓŚ·ŠĖ®£¬ŌņĶłÉÕ±ÖŠ¼ÓČė·ŠĖ®ŗóČÜŅŗÓÉ»ė×Ē±ä³ĪĒ壬
¹Ź“š°øĪŖ£ŗČÜŅŗÓÉ»ė×Ē±ä³ĪĒ壮
µćĘĄ ±¾Ģāæ¼²éĮĖŠŌÖŹŹµŃé·½°øÉč¼Ę£¬Éę¼°ŅŅ“¼µÄ“ß»ÆŃõ»Æ”¢±½·ÓµÄ»ÆѧŠŌÖŹµČÖŖŹ¶£¬ĢāÄæÄѶČÖŠµČ£¬Ć÷Č·ŅŅ“¼”¢±½·ÓµÄ»ÆѧŠŌÖŹĪŖ½ā“š¹Ų¼ü£¬ŹŌĢā³ä·Öæ¼²éѧɜµÄ·ÖĪö”¢Ąķ½āÄÜĮ¦¼°»ÆѧŹµŃéÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
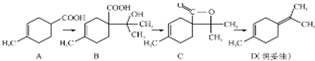 ŗśĶ×ÓĶ£ØD£©ÓĆ×÷ĻćĮĻµÄŌĮĻ£¬ĖüæÉÓÉAŗĻ³ÉµĆµ½£ŗ
ŗśĶ×ÓĶ£ØD£©ÓĆ×÷ĻćĮĻµÄŌĮĻ£¬ĖüæÉÓÉAŗĻ³ÉµĆµ½£ŗ| A£® | °“ĻµĶ³ĆüĆū·ØÓŠ»śĪļAµÄĆū³ĘĪŖ3-¼×»ł-3-»·ŅŃĻ©¼×Ėį | |
| B£® | Čē¹ūĢõ¼žŗĻŹŹ£¬BæÉÄÜ·¢Éś¼Ó¾Ū·“Ó¦£¬Ņ²æÉÄÜ·¢ÉśĖõ¾Ū·“Ó¦ | |
| C£® | C µÄ·Ö×ÓŹ½ĪŖC10H14O2 | |
| D£® | D ÓėBr2µÄCCl4ČÜŅŗ·“Ó¦£¬×ī¶ąÓŠ4ÖÖÉś³ÉĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀĻĀ£¬28g C2H4ÖŠŗ¬ÓŠµÄ¼«ŠŌ¹²¼Ū¼üŹżĪŖ6NA | |
| B£® | ŌŚĒāŃõ»Æ±µČÜŅŗÖŠ¼ÓČėÉŁĮæµÄĮņĖįĒāÄĘČÜŅŗ£ŗBa2++2OH-+2H++SO42-ØTBaSO4”ż+2H2O | |
| C£® | ÅØ¶Č¾łĪŖ0.1 mol•L-1µÄC6H5ONaČÜŅŗŗĶCH3COONaČÜŅŗÖŠ£ŗŅõĄė×ÓµÄ×ÜÅضČĒ°Õߊ”ÓŚŗóÕß | |
| D£® | ³£ĪĀĻĀ£¬ÅØ¶Č·Ö±šĪŖ0.1 mol•L-1ŗĶ0.01 mol•L-1µÄCH3COOHČÜŅŗÖŠ£ŗCH3COO-Ąė×ÓÅضČĒ°ÕߏĒŗóÕßµÄ10±¶ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŃÖŖH2µÄ±ź×¼Č¼ÉÕČČ”÷H=-285.8 kJ•mol-1£¬ŌņÓĆČČ»Æѧ·½³ĢŹ½æɱķŹ¾ĪŖ£ŗ H2£Øg£©+1/2O2£Øg£©ØTH2O£Øg£©”÷H=-285.8 kJ•mol-1 | |
| B£® | ÓĆ×ćĮæKMnO4ČÜŅŗĪüŹÕSO2ĘųĢå£ŗ2MnO4-+5SO2+2H2OØT2Mn2++5SO42-+4H+ | |
| C£® | NH4HSO3ČÜŅŗÓė×ćĮæNaOHČÜŅŗ¹²ČČ£ŗNH4++H++2OH-$\frac{\underline{\;\;”÷\;\;}}{\;}$NH3”ü+2H2O | |
| D£® | NaClOČÜŅŗÓėFeCl2ČÜŅŗ»ģŗĻ£ŗFe2++2ClO-+2H2OØTFe£ØOH£©2”ż+2HClO |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ŅŃÖŖ£¬AŹĒ³£¼ūµÄ½šŹōµ„ÖŹ£¬ÓėBµÄĖ®ČÜŅŗ·“Ӧɜ³ÉCŗĶD£®D”¢FŹĒĘųĢåµ„ÖŹ£¬DŌŚFÖŠČ¼ÉÕŹ±²śÉś²Ō°×É«»šŃę£®A”¢B”¢C”¢D”¢E”¢FĮłÖÖĪļÖŹµÄĻą»„×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾£Ø·“Ó¦Ģõ¼ž¼°²æ·Ö²śĪļĪ“ĮŠ³ö£©
ŅŃÖŖ£¬AŹĒ³£¼ūµÄ½šŹōµ„ÖŹ£¬ÓėBµÄĖ®ČÜŅŗ·“Ӧɜ³ÉCŗĶD£®D”¢FŹĒĘųĢåµ„ÖŹ£¬DŌŚFÖŠČ¼ÉÕŹ±²śÉś²Ō°×É«»šŃę£®A”¢B”¢C”¢D”¢E”¢FĮłÖÖĪļÖŹµÄĻą»„×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾£Ø·“Ó¦Ģõ¼ž¼°²æ·Ö²śĪļĪ“ĮŠ³ö£©²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś | B£® | ¢Ł¢Ü | C£® | ¢Ś¢Ū | D£® | ¢Ū¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ź×¼×“æöĻĀ£¬22.4 L HClČÜÓŚĖ®ŗóČÜŅŗÖŠŗ¬ÓŠnAøöHCl·Ö×Ó | |
| B£® | 1L 0.1 mol•L-1µÄNa2SO4ČÜŅŗÖŠŗ¬ÓŠ0.2 nAøöNa+ | |
| C£® | 1 mol ĮņĖį¼ŲÖŠŅõĄė×ÓĖł“ųµēŗÉŹżĪŖnA | |
| D£® | ½«0.1molĀČ»ÆĢśČÜÓŚ1LĖ®ÖŠ£¬ĖłµĆČÜŅŗŗ¬ÓŠ0.1nAFe3+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2 | B£® | 3 | C£® | 4 | D£® | 5 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com