



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| O2 |
| �� |
| O2 |
| �� |
| H2O |
| �� |
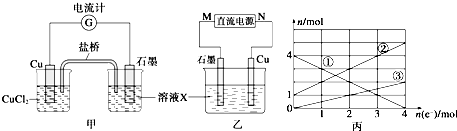
| A����XΪN2��NH3����AΪ���� |
| B����XΪS��H2S����AΪ���� |
| C����XΪ�ǽ������ʻ�ǽ����⻯���A��һ���������ͭ��Ӧ����Y |
| D����Ӧ�ٺ�һ��Ϊ������ԭ��Ӧ����Ӧһ��Ϊ��������ԭ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���Ʊ����ά |
| B�������ֻ�ҶƬ |
| C����������ģ�� |
| D��������ͻ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��483.6 kJ |
| B��88 kJ |
| C��285.8 kJ |
| D��44 kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ص��ܷ�Ӧ�ǣ�2CH3OH+3O2=2CO2+4H2O |
| B�������ķ�ӦΪ��O2+4H++4e-=2H2O |
| C�������ķ�ӦΪ��CH3OH+H2O-6e-=CO2��+6H+ |
| D����ع���ʱ��H+���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����λʱ��������amolA2��ͬʱ����2amolAB |
| B�������е���ѹ����ʱ����仯 |
| C��A2��B2��ABŨ�Ȳ���ʱ����仯 |
| D��v��A2����v��B2����v��AB��=1��1��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
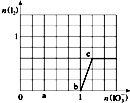 ��֪����ԭ��HSO3-��I-��������IO3-��I2���ں�3mol NaHSO3����Һ����μ���KIO3��Һ������KIO3������I2�����ʵ����Ĺ�ϵ������ͼ��ʾ���������й�˵����ȷ���ǣ�������
��֪����ԭ��HSO3-��I-��������IO3-��I2���ں�3mol NaHSO3����Һ����μ���KIO3��Һ������KIO3������I2�����ʵ����Ĺ�ϵ������ͼ��ʾ���������й�˵����ȷ���ǣ�������| A��b��ʱ�Ļ�ԭ���������I2 |
| B����n��KIO3��=1.1molʱ����Һ��n��I-��=0.5mol |
| C��a��ʱʣ��NaHSO3�����ʵ���Ϊ1.2mol |
| D����Ӧ�����е�������Ӧ���ò����ΪSO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1mol O |
| B��1mol O2 |
| C��1mol������ |
| D��1Ħ��ƻ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com