
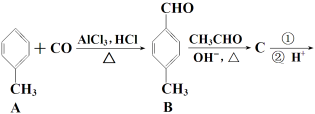
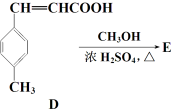
【题目】【化学 — 有机化学基础】3-对甲苯丙烯酸甲酯(E)是一种用于合成抗血栓药的中间体,其合成路线如下:
已知:HCHO+CH3CHO![]() CH2===CHCHO+H2O
CH2===CHCHO+H2O
(1) A的核磁共振氢谱图显示峰的面积比为_________;A→B新生成的官能团名称为 。
(2) B的同系物G(C9H10O)的同分异构体有多种,其中满足下列条件的同分异构体数目有 种(不考虑立体异构)① 遇FeCl3溶液呈紫色;②苯环上有两个取代基。
(3) C的结构简式为___________;D→E的反应类型为___________。
(4) 过程①选用的试剂可选用下列中的___________。
a.溴水 b. 银氨溶液 c.酸性KMnO4溶液 d.新制Cu(OH)2悬浊液
(5) ![]() 是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为__________________________。
是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为__________________________。
(6) E在一定条件下可以合成高聚物F,F的结构简式为___________。
【答案】(1)1:2:2:3(4种H原子数目正确即可得分)(2分);醛基(1分)
(2)9(2分)
(3)![]() (2分);取代反应(或酯化反应)(1分)
(2分);取代反应(或酯化反应)(1分)
(4)bd(漏选:1个选项正确得1分;错选:有错误选项得0分)(2分)(5)
(6) (2分)
(2分)
【解析】
试题分析:由合成路线可知,甲苯与CO反应生成A为对甲基苯甲醛,对甲基苯甲醛再与CH3CHO在碱性条件下反应: +CH3CHO
+CH3CHO![]()
 +H2O,①中-CHO被弱氧化剂氧化为-COOH,而碳碳双键不能被氧化,如与新制的氢氧化铜反应,被氧化成
+H2O,①中-CHO被弱氧化剂氧化为-COOH,而碳碳双键不能被氧化,如与新制的氢氧化铜反应,被氧化成 ,发生酯化反应:
,发生酯化反应: +CH3OH
+CH3OH![]()
 +H2O。
+H2O。
(1)根据A的结构简式可知,A中核磁共振氢谱图显示峰的面积比为1:2:2:3;A→B新生成的官能团名称为醛基;
(2) B的同系物G(C9H10O)的同分异构体有多种,遇FeCl3溶液呈紫色,说明含有酚羟基;②苯环上有两个取代基,则另一个取代基是丙烯形成的,丙烯分子中含有3类氢原子,则相应烃基有3种,和酚羟基的位置均有邻、间、对3种,共计9种;
(3)根据以上分析可知C的结构简式为![]() ;D→E的反应类型为取代反应;
;D→E的反应类型为取代反应;
(4)a.溴水能和碳碳双键加成,也能氧化醛基,a错误;b.银氨溶液为弱氧化剂,只能氧化醛基为羧基,b正确;c.酸性KMnO4溶液为强氧化剂,既能氧化碳碳双键,又能氧化醛基,c错误;d.新制Cu(OH)2悬浊液为弱氧化剂,只能氧化醛基为羧基,d正确,答案选bd。
(5)E同分异构体中含-COOC-,与足量NaOH溶液共热的化学方程式为
 。
。
(6)E分子中含有碳碳双键,在一定条件下可以生成高聚物F,发生加聚反应,则F的结构简式为 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】 橡胶是重要的工业原料,生胶的弹性好但强度较差,将其硫化后,强度增大则弹性减弱,且硫化程度越高,强度越大,弹性越差。在以下橡胶制品中,你认为硫化程度最高的是( )
A.气球 B.医用乳胶手套 C.汽车外胎 D.橡皮筋
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是( )
A.某ⅡA族元素的原子序数为a,则原子序数为a+1的元素一定是ⅢA族元素
B.除短周期外,其他周期均有32种元素
C.原子最外层只有2个电子的元素可能是金属元素也可能是非金属元素
D.碱金属元素是指ⅠA族的所有元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是( )
A. 氯化铝溶液中加入过量氨水:Al3++4NH3·H2O = AlO2-+4NH4++2H2O
B. 二氧化锰和浓盐酸共热:MnO2+2H++2Cl-![]() Mn2++Cl2↑+H2O
Mn2++Cl2↑+H2O
C. 漂白粉溶液中通入二氧化碳:Ca(ClO)2+H2O+ CO2==CaCO3+2HClO
D. 氯化亚铁溶液中通入氯气:2Fe2++Cl2 = 2Fe3++2Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】密闭容器中,由H2和CO直接制备二甲醚(CH3OCH3),其过程包含以下反应:
i.CO(g)+2H2(g)![]() CH3OH(g) H1=90.1kJ·mol1
CH3OH(g) H1=90.1kJ·mol1
ii.2CH3OH(g)![]() CH3OCH3(g)+H2O(g) H2=24.5kJ·mol1
CH3OCH3(g)+H2O(g) H2=24.5kJ·mol1
当其他条件相同时,由H2和CO直接制备二甲醚的反应中,CO平衡转化率随条件X 的变化曲线如右图所示。下列说法正确的是
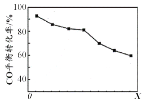
A . 由H2和CO直接制备二甲醚的反应为放热反应
B. 条件X为压强
C. X增大,二甲醚的产率一定增大
D. X增大,该反应的平衡常数一定减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由下列实验事实得出的结论正确的是( )
A. 由SiO2不能与水反应生成H2SiO3,可知SiO2不是H2SiO3的酸酐
B. 由SiO2+2C![]() Si+2CO↑,可知碳的非金属性大于硅
Si+2CO↑,可知碳的非金属性大于硅
C. CO2通入Na2SiO3溶液产生白色沉淀,可知酸性H2CO3>H2SiO3
D. SiO2可与NaOH溶液反应,也可与氢氟酸反应,可知SiO2为两性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电离度表示电解质的相对强弱,电离度的定义:
α=(已电离的电解质分子数/溶液中原有电解质的总分子数)×100%。
已知25℃时几种物质(微粒)的电离度(溶液浓度均为0.1 mol·L-1)如下表:
编号 | 物质(微粒) | 电离度α |
A | 硫酸溶液(第一步完全电离):第二步HSO4- | 10% |
B | 硫酸氢钠溶液:HSO4- | 29% |
C | 醋酸:CH3COOH | 1.33% |
D | 盐酸:HCl=H++Cl- | 100% |
(1)25℃时,0.1 mol·L-1上述几种溶液中,c(H+)从小到大的顺序是 (填序号);
(2)25℃时,0.1 mol·L-1硫酸溶液中HSO4-的电离度小于相同温度下0.1 mol·L-1硫酸氢钠溶液中HSO4-的电离度,其原因是 。
(3)醋酸的电离平衡常数K的表达式是 ,醋酸的电离平衡常数K与电离度α的关系式为:K= (用含α的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中每种物质都既有离子键又有共价键的一组是( )
A.NaOH、H2SO4、(NH4)2SO4
B.Ba(OH)2、Na2SO4、Na3PO4
C.Na2CO3、HNO3、MgO
D.HCl、Al2O3、MgCl2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com