
| A、镁产生的多 |
| B、铝产生的多 |
| C、镁和铝产生的一样多 |
| D、无法比较 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
A、铜与浓硝酸反应制NO2:可采用如图装置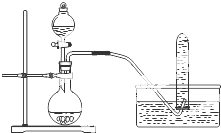 |
| B、分离乙酸和乙醇溶液:用分液漏斗进行分离 |
| C、稀硫酸和锌粒反应制取氢气:加入少许硫酸铜以加快反应速率 |
| D、鉴别Na2CO3溶液和NaHCO3溶液:分别向两种溶液滴加澄清石灰水至过量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、M |
| B、M2+ |
| C、M3+ |
| D、MO2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
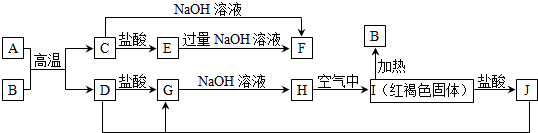
查看答案和解析>>
科目:高中化学 来源: 题型:
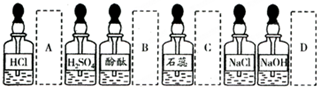
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、俗名是苏打 |
| B、相同温度下溶解度比Na2CO3大 |
| C、热稳定性比Na2CO3好 |
| D、能与酸反应放出CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| MnO2 |
| 加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaOH+HCl═NaCl+H2O | ||||
| B、H2CO3═H2O+CO2 | ||||
C、H2+CuO
| ||||
D、2CO+O2
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com