
 2SO3(g),当其他条件不变时,只改变一个反应条件,将生成的S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”).
2SO3(g),当其他条件不变时,只改变一个反应条件,将生成的S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”).| 编号 | 改变的条件 | 生成SO3一的速率 |
| ① | 升高温度 | 增大 增大 |
| ② | 降低温度 | 减小 减小 |
| ③ | 增大氧气的浓度 | 增大 增大 |
| ④ | 使用催化剂 | 增大 增大 |
| ⑤ | 压缩体积 | 增大 增大 |


科目:高中化学 来源: 题型:
 2SO3(g),当其他条件不变时,只改变一个反应条件,将生成的S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”).
2SO3(g),当其他条件不变时,只改变一个反应条件,将生成的S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”).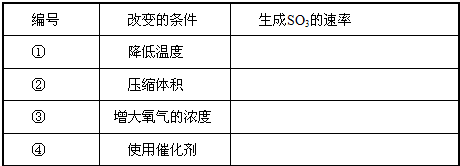
查看答案和解析>>
科目:高中化学 来源:2011-2012学年辽宁省盘锦市二中高一下学期期中考试化学试卷(带解析) 题型:填空题
(6分)对于反应2S02+02 2SO3(g)当其他条件不变时,只改变一个反应条件,将生成的S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”)。
2SO3(g)当其他条件不变时,只改变一个反应条件,将生成的S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”)。
| 编号 | 改变的条件 | 生成SO3的速率 |
| ① | 升高温度 | |
| ② | 降低温度 | |
| ③ | 增大氧气的浓度 | |
| ④ | 使用催化剂 | |
| ⑤ | 压缩体积 | |
| ⑥ | 恒容下充人Ne | |
查看答案和解析>>
科目:高中化学 来源:2014届辽宁省盘锦市高一下学期期中考试化学试卷(解析版) 题型:填空题
(6分)对于反应2S02+02 2SO3(g)当其他条件不变时,只改变一个反应条件,将生成的S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”)。
2SO3(g)当其他条件不变时,只改变一个反应条件,将生成的S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”)。
|
编号 |
改变的条件 |
生成SO3的速率 |
|
① |
升高温度 |
|
|
② |
降低温度 |
|
|
③ |
增大氧气的浓度 |
|
|
④ |
使用催化剂 |
|
|
⑤ |
压缩体积 |
|
|
⑥ |
恒容下充人Ne |
|
查看答案和解析>>
科目:高中化学 来源: 题型:
(12分)(1)某温度时,在4 L容器中X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。由图中数据分析,该反应的化学方程式为 。
反应开始至2min,Z的平均反应速率为 。若X、Y、Z均为气体,反应达平衡时:此时体系的压强是开始时的 倍。
(2)对于反应2S02+02![]() 2SO3(g),当其他条件不变时,只改变一个反应条件,将生成S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”)。
2SO3(g),当其他条件不变时,只改变一个反应条件,将生成S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”)。
编号 | 改变的条件 | 生成SO3的速率 |
① | 升高温度 |
|
② | 降低温度 |
|
③ | 增大氧气的浓度 |
|
④ | 使用催化剂(正) |
|
⑤ | 压缩体积 |
|
⑥ | 减少S02的浓度 |
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com