
【题目】CO、H2、CH3OH均是清洁能源。
(1)已知部分化学键键能数据如下:
化学键 | C | O=O | C=O | C-O |
E/(kJ mol-1) | 958.5 | 497 | 745 | 351 |
2CO(g) +O2(g)==2CO2(g) ![]() H1 H2O(g)+CO(g)==H2(g) + CO2(g)
H1 H2O(g)+CO(g)==H2(g) + CO2(g) ![]() H2 = -41 kJmol-1
H2 = -41 kJmol-1
CH3OH(g)+ 3/2O2(g)==CO2(g)+2H2O(g) ![]() H3 = -660kJmol-1
H3 = -660kJmol-1
则△H1=_____ kJmol-1,反应CO(g)+2H2(g)![]() CH3OH(g)的△H=_____ kJmol-1。
CH3OH(g)的△H=_____ kJmol-1。
(2)一定条件下,在容积为2 L的密闭容器Q中充入a mol CO与b molH2合成甲醇:CO(g) +2H2(g) ![]() CH3OH(g)。测得平衡时混合气体中CH3OH的体积百分含量与温度、 压强之间的关系如图1所示,图2表示在一定温度下,H2的平衡转化率与反应开始时两种反应物的投料物质的量之比(用X表示)、压强之间的关系。
CH3OH(g)。测得平衡时混合气体中CH3OH的体积百分含量与温度、 压强之间的关系如图1所示,图2表示在一定温度下,H2的平衡转化率与反应开始时两种反应物的投料物质的量之比(用X表示)、压强之间的关系。

①压强相同时,温度为T1、T2时,反应达到平衡所需要的时间分别为t1、t2,则二者之间的相对大小为t1___ t2(填“>”、“<”、“=”或“无法确定”)。
②P1_____P2(填“>”、“<”、“=”或“无法确定”)。
③若a =2,b=4,则压强为P1、温度为T1时该反应的平衡常数K=______________。
④若在压强为P1、温度为T1时,向Q容器中同时加入等物质的量的CO、H2、CH3OH三种气体,则反应开始时,v(CH3OH)正_____v(CH3OH)逆(填“>”、“<”、“=”或“无法确定”)。
【答案】-566 -107 > > 4.5 无法确定
【解析】
(1)根据化学方程式及化学键键能数据,![]() H1
H1![]() ;根据盖茨定律,CO(g)+2H2(g)
;根据盖茨定律,CO(g)+2H2(g)![]() CH3OH(g)的
CH3OH(g)的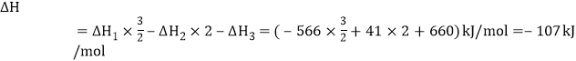 ,故本小题答案为:-566;-107;
,故本小题答案为:-566;-107;
(2)①因为CO(g) +2H2(g)![]() CH3OH(g) △H=-107kJmol-1,所以温度越高,平衡时CH3OH的含量越低,所以图1中T2>T1,压强相同、温度为T1、T2时,反应达到平衡所需要的时间分别为t1、t2,则二者的相对大小关系为t1>t2,本小题的答案为:>;
CH3OH(g) △H=-107kJmol-1,所以温度越高,平衡时CH3OH的含量越低,所以图1中T2>T1,压强相同、温度为T1、T2时,反应达到平衡所需要的时间分别为t1、t2,则二者的相对大小关系为t1>t2,本小题的答案为:>;
②已知a mol CO与b molH2合成甲醇,故投料物质的量之比(用X表示)为:![]() ;由图2知,投料比相同时,压强为P1时氢气平衡转化率高,又因为该反应正向为气体体积减小的反应,故P1>P2,本小题答案为:>;
;由图2知,投料比相同时,压强为P1时氢气平衡转化率高,又因为该反应正向为气体体积减小的反应,故P1>P2,本小题答案为:>;
③若a=2,b=4,则压强为P1、温度为T1时,列三段式:
CO(g) +2H2(g)![]() CH3OH(g)
CH3OH(g)
开始(mol)2 4 0
转化(mol)x 2x x
平衡(mol)2-x 4-2x x
由图1,此条件下平衡时CH3OH的体积分数为40%,所以:![]() ,解得
,解得![]() ,所以平衡时n(CO)=
,所以平衡时n(CO)=![]() mol,n(H2)=
mol,n(H2)=![]() mol,又因为容积为2L,所以CO、H2、CH3OH的平衡浓度分别为:
mol,又因为容积为2L,所以CO、H2、CH3OH的平衡浓度分别为:![]() mol·L-1、
mol·L-1、![]() mol·L-1、
mol·L-1、![]() mol·L-1,故
mol·L-1,故![]() ,本小题答案为:4.5;
,本小题答案为:4.5;
④若在压强为P1、温度为T1时,向Q容器中同时加入等物质的量的CO、H2、CH3OH三种气体(设为y),此时浓度商=![]() ,与K无法比较大小,不能确定平衡向哪个方向移动,故无法确定ν(CH3OH)正与ν(CH3OH)逆的大小。
,与K无法比较大小,不能确定平衡向哪个方向移动,故无法确定ν(CH3OH)正与ν(CH3OH)逆的大小。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】设用NA表示阿伏加德罗常数的值,其计算近似值为6.02×1023,按要求完成下列填空:
①0.5mol NH3共含有____个原子。
②6mol H2O与标准状况下___LNH3所含氢原子数相等。
③某硫酸钠溶液中含有3.01×1022个Na+,则该溶液中SO42-的物质的量是____。
④标准状况下11.2L NO和____g NO2所含有的氧原子数相等。
⑤0.8g某物质含有3.01×1022个分子,该物质的相对分子质量约为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组拟探究锡及锡的化合物的部分性质。经查阅资料知:Sn的熔点231℃;SnCl2易被氧化,且易水解;Sn(OH)2常温下易分解,SnCl4常温下为无色液体,熔点-33℃,沸点114.1℃,请回答下列问题:
(1)该小组用以下流程制备SnSO4晶体:

①操作Ⅱ所需的实验仪器为______________________________________________。
②过滤操作中玻璃棒使用的注意事项为____________________________。
③操作Ⅰ为沉淀的洗涤。请简述如何判断沉淀是否洗涤干净:____________________。
(2)用熔融的锡与干燥的氯气制备SnCl4,提供的装置如下:

①装置Ⅲ为冷凝管,则水流从________进入。
②请用大写英文字母按从左到右顺序连接组装仪器_________________________________________。
③有同学指出②中连接的实验装置存在不足,不足之处为______________________。
(3)测定锡粉质量分数的步骤:取锡粉1.226g溶于盐酸中,加入过量的FeCl3溶液,再用0.1000mol·L1 K2Cr2O7溶液滴定Fe2+,消耗K2Cr2O7溶液32.00mL,发生的反应:6FeCl2+K2Cr2O7+
14HCl===6FeCl3+2KCl+2CrCl3+7H2O。则锡粉的质量分数为(杂质不参与反应)____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO3,还含有少量MgO、SiO2等杂质)来制备,工艺流程如下:

回答下列问题:
(1)“酸浸”实验中,铁的浸出率结果如上图所示。由图可知,当铁的浸出率为70%时,所采用的实验条件为_____________。
(2)“酸浸”后,钛主要以![]() 形式存在,写出相应反应的离子方程式________。
形式存在,写出相应反应的离子方程式________。
(3)TiO2·xH2O沉淀与双氧水、氨水反应40 min所得实验结果如下表所示:

分析40 ℃时TiO2·xH2O转化率最高的原因________。
(4)Li2Ti5O15中Ti的化合价为+4,其中过氧键的数目为_______。
(5)若“滤液②”中![]() ,加入双氧水和磷酸(设溶液体积增加1倍),使
,加入双氧水和磷酸(设溶液体积增加1倍),使![]() 恰好沉淀完全即溶液中
恰好沉淀完全即溶液中![]() ,此时是否有
,此时是否有![]() 沉淀生成? ________(列式计算)。
沉淀生成? ________(列式计算)。![]() 的Ksp分别为
的Ksp分别为![]()
(6)写出“高温煅烧②”中由![]() 制备
制备![]() 的化学方程式___________。
的化学方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式正确的是( )
A. 醋酸溶于水:CH3COOH===CH3COO-+H+
B. NaHSO4溶于水:NaHSO4===Na++HSO4-
C. 碳酸氢钠溶于水:NaHCO3![]() HCO
HCO![]() +Na+
+Na+
D. 次氯酸溶于水:HClO![]() H++ClO-
H++ClO-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮是植物体内蛋白质、叶绿素的重要组成元素,氮肥能促进农作物的生长。氨是生成氮肥的原料。回答下列问题:
(1)氮气的电子式________________ ,氨的结构式__________________;
(2)氨水显碱性,写出氨水的电离方程式___________________________________________;
(3)氨催化氧化生成NO是工业制硝酸的反应之一,写出该反应的化学方程式:________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸是三大工业用酸之一,在冶金、石油工业、制药、国防等方面都要用到硫酸。将适量的蔗糖放入烧杯中,加少量水拌匀,再加适量浓硫酸,迅速搅拌,放出大量的热,同时观察到蔗糖逐渐变黑,体积膨胀,并放出有刺激性气味的气体。试回答:
(1)加入少量水的原因是_________________________________________________。
(2)生成的黑色物质是______________(写出化学式)。
(3)“体积膨胀,并放出有刺激性气味的气体(SO2)”,写出对应的化学方程式:_________________________________________________。
(4)上述现象体现了浓硫酸的_________________(填序号)
①酸性 ②吸水性 ③脱水性 ④强氧化性
(5)向80mL浓硫酸中加入5.6g铜,加热一段时间后至不再反应为止,实验测得反应中共有1.12L(标准状况下)SO2气体生成,该反应的化学方程式为_____________________________________,反应中转移电子______mol,铜剩余_______g,该反应中浓硫酸体现了___________和__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中H2SO4、NaOH是两种常见试剂。
(1)现在实验室中有一瓶98%的H2SO4(ρ=1.84g/cm3)。
①该硫酸的物质的量浓度为____________mol/L;
②现要配置2.0mol/L的稀H2SO4250mL,请回答如下问题:需要量取浓硫酸的体积为________(保留一位小数).在该实验使用的玻璃仪器中除烧杯、玻璃棒、胶头滴管、量筒外,还有__________。
(2)有一瓶氢氧化钠固体由于放置时间较长,某同学怀疑其由于吸收空气中CO2而发生部分变质。为证明此推测,进行如下实验。
称取2.000g样品,配制成250mL待测液。量取20.00mL待测液,当慢慢滴入0.100mol/L的硫酸溶液18.60mL时测得溶液正好显中性.根据实验数据可知:
待测溶液中氢氧化钠的浓度为_____________mol/L;
样品中氢氧化钠的质量百分数为______________。
由此,该同学得出结论:样品已部分变质.
①请你对实验进行评价(假定实验操作过程准确无误):_________
A.该实验不能证明关于“部分变质”的推测
B.该实验可以证明关于“部分变质”的推测
C.若样品中混有少量氢氧化钾,也能使其质量百分数变小
②在用氢氧化钠固体配制溶液过程中,下列操作中也会造成氢氧化钠质量百分数偏小的是________(填字母)。
A.在称量时,把氢氧化钠样品放在称量纸上进行称量
B.在溶解过程中,有少量液体溅出
C.在转移过程中,烧杯和玻璃棒没有进行洗涤
D.在定容时,滴加蒸馏水超过刻度线,用滴管从容量瓶中小心取出多余液体至液体凹液面与刻度线水平
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为T时,向2.0L恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g)![]() PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:下列说法正确的是
PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:下列说法正确的是
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/ mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
A.反应在前50 s的平均速率为v(PCl3)=0.0032mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时c(PCl3)=0.11mol·L-1,则反应的△H<0
C.相同温度下,起始时向容器中充入1.0mol PCl5、0.20mol PCl3和0.20molCl2,达到平衡前v(正)>v(逆)
D.相同温度下,起始时向容器中充入2.0mol PCl3和2.0molCl2,达到平衡时,PCl3的转化率小于80%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com