
| A. | 乙烯的结构式: | B. | 钠离子的结构示意图: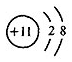 | ||
| C. | 氢分子的电子式:H:H | D. | 氯化氢分子的电子式: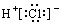 |
分析 A.用短线“-”代替所有的共用电子对即为结构式;
B.钠离子的核电荷数为11,核外电子总数为10,最外层达到8电子稳定结构;
C.氢气分子中含有1个碳碳双键,碳原子最外层满足2电子稳定结构;
D.HCl分子为共价化合物,分子中不存在阴阳离子.
解答 解:A.乙烯分子中含有1个碳碳双键,为平面结构,其结构式为: ,故A正确;
,故A正确;
B.钠离子最外层满足8电子稳定结构,其离子结构示意图为: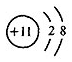 ,故B正确;
,故B正确;
C.氢分子为共价化合物,其分子中含有1个H-H键,其电子式为H:H,故C正确;
D.氯化氢为共价化合物,其电子式中不能标出电荷,氯化氢正确的电子式为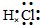 ,故D错误;
,故D错误;
故选D.
点评 本题考查了常见化学用语的表示方法,题目难度不大,涉及离子结构示意图、结构式、电子式等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的规范答题能力.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t/min | X/mol | Y/mol | Z/mol |
| 0 | 1.00 | 2.00 | 0.00 |
| 1 | 0.90 | 1.80 | 0.20 |
| 3 | 0.75 | 1.50 | 0.50 |
| 5 | 0.65 | 1.30 | 0.70 |
| 9 | 0.55 | 1.10 | 0.90 |
| 10 | 0.55 | 1.10 | 0.90 |
| 14 | 0.55 | 1.10 | 0.90 |
 2Z
2Z查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在任何条件下,纯水的pH=7 | |
| B. | 盐类对水的电离都有促进作用 | |
| C. | 在95℃时,纯水的pH>7 | |
| D. | 在95℃时,纯水中H+的物质的量浓度c(H+)>10-7mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
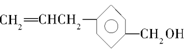 ,下列关于有机物A的说法错误的是( )
,下列关于有机物A的说法错误的是( )| A. | 有机物A可以与氯气反应 | |
| B. | 有机物A与 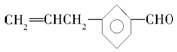 互为同分异构体 互为同分异构体 | |
| C. | 有机物A可与CH3COOH发生酯化反应 | |
| D. | 有机物A可以使酸性KMnO4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 容器 | 甲 | 乙 | 丙 |
| 反应物的投入量 | 1molN2、3molH2 | 2molNH3 | 4molNH3 |
| NH3的浓度(mol•L-1) | c1 | c2 | c3 |
| 反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
| 体系的压强(Pa) | p1 | p2 | p3 |
| 反应物的转化率 | a1 | a2 | a3 |
| A. | a+b=92.4 | B. | 2c1>c3 | C. | 2p2<p3 | D. | α1+α3=1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com