
【题目】高锰酸钾可用于生活消毒,是中学化学常见的氧化剂。工业上,用软锰矿(主要成分是二氧化锰)制高锰酸钾的流程如下(部分条件和产物省略):
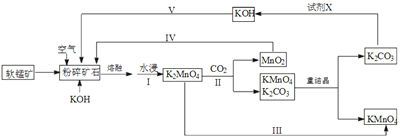
请回答下列问题:
(1)提高锰酸钾浸出率(浸出锰酸钾质量与固体总质量之比)的措施有______________________。
(2)写出向二氧化锰和氢氧化钾熔融物中通入空气时发生的主要化学反应的方程式:___________________________________。
(3)从经济性考虑试剂X宜选择(填名称):___________。上述流程中,设计步骤IV和V的目的是____________________________________。
(4)以惰性材料为电极,采用电解锰酸钾溶液的方法完成步骤III转化。
①阳极反应式为___________________。
②电解过程中,阴极附近电解质溶液的pH将_______(填:增大、减小或不变)。
(5)测定高锰酸钾样品纯度:向高锰酸钾溶液中滴定硫酸锰溶液,产生黑色沉淀。当溶液由紫红色刚好褪色且半分钟不变色时,达到滴定终点。写出离子方程式:__________________。
(6)已知:常温下,Ksp [Mn(OH)2]=2.010-13。工业上,调节pH沉淀废水中Mn2+。当pH=10时,溶液中c(Mn2+)=______________。
【答案】加热、搅拌等 2MnO2+4KOH+O2![]() 2K2MnO4+2H2O 石灰乳(或生石灰) 循环利用二氧化锰、氢氧化钾,提高原料利用率 MnO42--e-=MnO4- 2MnO4-+3Mn2++2H2O=5MnO2↓+4H+ 增大 2.0×10-5mol/L
2K2MnO4+2H2O 石灰乳(或生石灰) 循环利用二氧化锰、氢氧化钾,提高原料利用率 MnO42--e-=MnO4- 2MnO4-+3Mn2++2H2O=5MnO2↓+4H+ 增大 2.0×10-5mol/L
【解析】
(1)为提高提高锰酸钾浸出率,应采用加热、搅拌的方法,使反应尽可能多的生成锰酸钾;
(2)根据流程图,二氧化锰与氢氧化钾溶液、氧气在高温条件下发生反应生成锰酸钾和水,化学方程式为2MnO2+4KOH+O2![]() 2K2MnO4+2H2O;
2K2MnO4+2H2O;
(3)碳酸钾与X反应又得氢氧化钾,所以X试剂应是与碳酸钾发生复分解反应的物质,结合碳酸根离子的性质判断X是石灰乳或生石灰;设计步骤IV和V的目的是使氢氧化钾、二氧化锰重新被利用,提高原料的利用率;
(4)锰酸钾生成高锰酸钾,Mn元素的化合价升高,所以锰酸钾发生氧化反应,所以电解锰酸钾溶液的阳极反应式为锰酸根离子失去电子生成高锰酸根离子,电极反应式为MnO42--e-=MnO4-;阴极是氢离子放电生成氢气,氢离子浓度减小,氢氧根离子浓度增大,则溶液的pH增大;
(5)向高锰酸钾溶液中滴定硫酸锰溶液,产生黑色沉淀,该黑色沉淀是二氧化锰,所以该滴定反应的离子方程式为2MnO4-+3Mn2++2H2O=5MnO2↓+4H+;
(6)Mn(OH)2的溶度积Ksp=c(Mn2+)c(OH-)2=2.0×10-13,当pH=10时,c(OH-)=1.0×10-4mol/L,所以c(Mn2+)=2.0×10-13/ c(OH-)2=2.0×10-5mol/L.


 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:
【题目】
化合物G是治疗高血压的药物“比索洛尔”的中间体,一种合成G的路线如下:

已知以下信息:
①A的核磁共振氢谱为单峰;B的核磁共振氢谱为三组峰,峰面积比为6∶1∶1。
②D的苯环上仅有两种不同化学环境的氢;1molD可与1mol NaOH或2mol Na反应。
回答下列问题:
(1)A的结构简式为____________。
(2)B的化学名称为____________。
(3)C与D反应生成E的化学方程式为____________。
(4)由E生成F的反应类型为____________。
(5)G是分子式为____________。
(6)L是D的同分异构体,可与FeCl3溶液发生显色反应,1mol的L可与2mol的Na2CO3反应,L共有______种;其中核磁共振氢谱为四组峰,峰面积比为3∶2∶2∶1的结构简式为___________、____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅蓄电池是最早使用的充电电池。目前汽车上使用的电瓶大多数仍是铅蓄电池,其电池反应为:Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O,下列说法正确的是
2PbSO4+2H2O,下列说法正确的是
A.该电池放电过程中,溶液的pH值增大
B.放电时,电池的负极反应为:Pb-2e-= Pb2+
C.该电池的充、放电过程互为可逆反应
D.放电过程中,电子的流向为:负极→导线→正极→H2SO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,同体积的CO和CO2,下列说法不正确的是( )
A.分子数之比等于1∶1B.质量之比等于7∶11
C.密度之比等于1∶1D.中子数之比等于7∶11
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以色列理工学院的丹尼尔·谢德曼因“发现准晶体”而一人独享了2011年度诺贝尔化学奖。某组成为Al65Cu23Fe12的准晶体W具有低摩擦系数、高硬度、低表面能以及低传热性,正被开发为炒菜锅的镀层。下列有关说法中正确的是( )
A.W的熔点比铝、铁、铜的都高
B.将一定量W投入少量的盐酸中,充分反应后溶液中一定有Fe2+
C.等质量W分别与足量NaOH溶液、盐酸反应,生成氢气的质量之比为65:73
D.W在氯气中完全燃烧时可形成AlCl3、FeCl3两种离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学兴趣小组模拟利用氨气和次氯酸钠合成肼(N2H4)的过程。设计了如图装置:

(1)盛放浓盐酸的仪器名称是_______________。
(2)装置⑤中发生反应的化学方程式为____________________________________。
(3)在________(填图中的装置数字序号)装置中制备肼,发生反应的化学方程式为______________________________________________。
(4)②中盛装的试剂为_______________,作用是________________。
(5)肼是一种可燃性气体,可用作火箭燃料,与氧气或氮的氧化物反应时,生成物均无污染,写出肼和一氧化氮燃烧反应的化学方程式_____________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知高锰酸钾与浓盐酸在常温下反应能产生氯气。若用下图所示的实验装置来制备纯净、干燥的氯气,并实验其与金属的反应。每个虚线框表示一个单元装置,其中有错误的是( )

A.①和②处B.只有②处
C.②和③处D.②、③、④处
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求书写名称或结构简式:
(1)3-甲基-2-丙基-1-戊烯结构简式为________。
(2)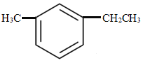 系统命名为________。
系统命名为________。
(3)![]() 的系统命名________。
的系统命名________。
(4)相对分子质量为72且支链最多的烷烃的结构简式______________ ;
(5)某烃经李比希元素分析实验测得碳的质量分数为85.71%,氢的质量分数为14.29%.该烃的质谱图显示其相对分子质量为70,该烃的核磁共振氢谱只有一个峰,请通过计算确定该烃的实验式________,分子式________,结构简式________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com