
| m |
| M |
| 12.6g |
| 18g/mol |
| 26.4g |
| 44g/mol |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 组合编号 | A的分子式 | B的分子式 | A和B的体积比VA:VB |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 规律 | 结论 |
| A | Cl2、Br2等卤素单质与水反应的化学方程式为:X2+H2O═HX+HXO | 氟气与水反应的化学方程式为:F2+H2O═HF+HFO |
| B | 两种活泼性不同的金属作原电池电极时,活泼金属作负极 | 镁、铝构成的原电池中,镁一定作负极 |
| C | 发生复分解反应要具备以下3个条件之一:生成难溶物、难电离物质或挥发性气体 | 在反应FeCl3+3KSCN═Fe(SCN)3+3KCl中,盐Fe(SCN)是弱电解质 |
| D | 加入与难溶盐含相同离子的强电解质时,难溶盐的溶解度会降低 | 为减少洗涤过程中固体的损失,应选用稀Na2SO4溶液代替H2O来洗涤BaSO4沉淀 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 向100mL NaOH溶液中通入CO2充分反应后,在减压和较低温度下,小心地将溶液蒸干,得到白色固体M.通入二氧化碳的体积V(标准状况下)与M的质量W的关系如图所示.请回答下列问题:
向100mL NaOH溶液中通入CO2充分反应后,在减压和较低温度下,小心地将溶液蒸干,得到白色固体M.通入二氧化碳的体积V(标准状况下)与M的质量W的关系如图所示.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铁有剩余 |
| B、反应中氧化产物与还原产物的质量之比为2:5 |
| C、往溶液滴入KSCN溶液显红色 |
| D、溶液中的Fe2+和Fe3+的物质的量之比为1:6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、x:y=1:1 |
| B、充分反应后,生成15.9 g Na2CO3 |
| C、充分反应后,生成0.25 mol Na2CO3 |
| D、生成氧气的过程中共转移电子0.15 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
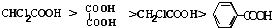 下列说法中不正确的是( )
下列说法中不正确的是( )A、等浓度等体积的4种酸中和碱的能力: |
B、等浓度的4种酸溶液中水电离出的c水(H+): >CH2ClCOOH> >CH2ClCOOH> >CHCl2COOH >CHCl2COOH |
C、反应 +2CH2ClCOO-→ +2CH2ClCOO-→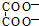 +2CH2ClCOOH一定能够发生 +2CH2ClCOOH一定能够发生 |
| D、由题中信息可推知酸性:CH2FCOOH>CH2ClCOOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com