
(1)用Cl2生产某些含氯有机物时会产生副产物HCl。
利用反应A可实现氯的循环利用。反应A:4HCl+O2 2Cl2+2H2O
2Cl2+2H2O
已知:ⅰ.此条件下反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。
ⅱ.

①写出此条件下,反应A的热化学方程式 。
②断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为 kJ。
(2)氢气用于工业合成氨 N2(g) + 3H2(g)  2NH3(g);ΔH = -92.2 kJ·mol-1。
2NH3(g);ΔH = -92.2 kJ·mol-1。
①一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,正逆反应速率与时间的关系如下图所示,其中t4 ﹑t5 ﹑t7时刻对应的实验条件改变分别是t4 ;t5 ;t7 。

②温度为T℃时,将2nmolH2和nmolN2放入0.5L密闭容器中,充分反应后测得N2的转化率为50﹪,此时放出热量46.1 kJ。则n= 。
(3)科学家用氮化镓材料与铜组装如图的人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4。
①写出铜电极表面的电极反应式 。
②为提高该人工光合系统的工作效率,可向装置中加入少量 (选填“氢氧化钠”或“硫酸”)。
(4)传统制备肼的方法是以NaClO氧化NH3,制得肼(N2H4)的稀 溶液。该反应的
溶液。该反应的 离子方程式是 。
离子方程式是 。
科目:高中化学 来源:2017届河北省高三上期中化学卷(解析版) 题型:选择题
20 ℃时,饱和NaCl溶液的密度为ρg·cm-3,物质的量浓度为c mol·L-1,则下列说法中不正确的是
A.温度低于20 ℃时,饱和NaCl溶液的浓度小于c mol·L-1
B.此溶液中NaCl的质量分数为 ×100%
×100%
C.20 ℃时,密度小于ρg·cm-3的NaCl溶液是不饱和溶液
D.20 ℃时,饱和NaCl溶液的溶解度S= g
g
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上月考三化学试卷(解析版) 题型:选择题
粗盐的提纯实验中,下列操作错误的是( )
A.蒸发过程中用玻璃棒不断搅拌
B.先用酒精灯加热蒸发皿,再将滤液倒入蒸发皿中
C.当加热至蒸发皿中有较多固体析出时停止加热,利用余热将液体蒸干
D.蒸发完成时,用 坩埚钳把蒸发皿移至石棉网上
坩埚钳把蒸发皿移至石棉网上
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高一上月考二化学卷(解析版) 题型:选择题
如图锥形瓶中装满了c mol/L的Na2SO4溶液,经测定其中含有 mol Na+,则锥形瓶容积为
mol Na+,则锥形瓶容积为

A. B.
B. C.
C. D.
D.
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高二上期中选修化学卷(解析版) 题型:选择题
下列各项叙述中,正确的是
A.分子晶体中不一定存在分子间作用力
B.价电子排布为4s24p1的元素位于第四周期第ⅠA族,是S区元素
C.已知金属钛的晶胞是面心立方结构(如图),则钛晶体1个晶胞中钛原子数为4个

D.水是一种非常稳定的化合物,这是由于氢键所导致
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高二上期中选修化学卷(解析版) 题型:选择题
在玻璃熔炉中,纯碱与石英反应生成Na2SiO3和CO2。下列说法正确的是
A.该反应是氧化还原反应 B.微粒的半径:r(Si)>r(Na)
C.Na2CO3中含有离子键和共价键 D.硅酸 的酸性强于碳酸
的酸性强于碳酸
查看答案和解析>>
科目:高中化学 来源:2017届湖南省高三上月考三化学试卷(解析版) 题型:选择题
下列有关反应热的叙述中正确的是
①已知2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ·mol-1,则氢气的燃烧热为△H=-241.8 kJ·mol-1
②由单质A转化为单质B是一个吸热过程,由此可知单质B比单质A稳定
③X(g)+Y(g) Z(g)+W(s) ΔH>0,恒温恒容条件下达到平衡后加入X,上述反应的ΔH增大
Z(g)+W(s) ΔH>0,恒温恒容条件下达到平衡后加入X,上述反应的ΔH增大
④已知:
共价键 | C—C | C===C | C—H | H—H |
键能/(kJ·mol-1) | 348 | 610 | 413 | 436 |
上表数据可以计算出 的焓变
的焓变
⑤根据盖斯定律,推知在相同条件下,金刚石或石墨燃烧生成1 mol CO2固体时,放出的热量相等
⑥25℃,101 kPa时,1 mol碳完全燃烧生成CO2所放出的热量为碳的燃烧热
A.①②③④ B.③④⑤ C.④⑤ D.⑥
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上期中化学试卷(解析版) 题型:填空题
工业生产中产生的废气、废液、废渣直接排放会造成污染,很多都经过吸收转化为化工产品。
I.利用电化学原理吸收工业生产中产生的SO2、NO,同时获得Na2S2O4和NH4NO3产品的工艺流程图如图(Ce为铈元素)。
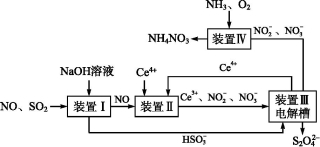
请回答下列问题:
(1)装置Ⅱ中NO在酸性条件下生成NO2-的离子方程式: 。
(2)装置Ⅲ的作用之一是再生Ce4+,其原理如下图所示:
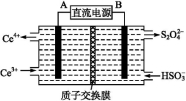
右侧反应室中发生的主要电极反应式为 。
(3)已知进入装置Ⅳ的溶液中NO2-的浓度为0.4 mol·L-1,要使1 m3该溶液中的NO2-完全转化为 NH4NO3,需至少向装置Ⅳ中通入标准状况下的O2的体积为 L。
II.以电石渣[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的流程如下:

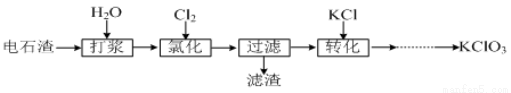
(4)氯化过程控制电石渣过量,在75℃左右进行。氯化时存在Cl2与Ca(OH)2作用生成Ca(ClO)2的反应,Ca(ClO)2进一步转化为Ca(ClO3)2,少量Ca(ClO)2 分解为CaCl2和O2。提高Cl2转化为Ca(ClO3)2的转化率的可行措施有 (填序号)。
A.适当减缓通入Cl2速率 B.充分搅拌浆料 C.加水使Ca(OH)2完全溶解
(5)氯化过程中Cl2 转化为Ca(ClO3)2的总反应方程式为
6Ca(OH)2+6Cl2===C a(ClO3)2+5CaCl2+6H2O
a(ClO3)2+5CaCl2+6H2O
氯化完成后过滤。滤渣的主要成分为 (填化学式)。
(6)向滤液中加入稍过量KCl固体可将Ca(ClO3)2转化为KClO3 ,若溶液中KClO3的含量为100g?L?1,从该溶液中尽可能多地析出KClO3固体的方法是 。
,若溶液中KClO3的含量为100g?L?1,从该溶液中尽可能多地析出KClO3固体的方法是 。

(7)工业上常用磷精矿[Ca5(PO4)3F]和硫酸反应制备磷酸。已知25℃,101kPa时:
CaO(s)+H2SO4(l)=CaSO4(s)+H2O(l) △H=-271kJ/mol
5CaO(s)+H3PO4(l)+HF(g)=Ca5(PO4)3F(s)+5H2O(l) △H=-937kJ/mol
则Ca5(PO4)3F和硫酸反应生成磷酸的热化学方程式是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com