
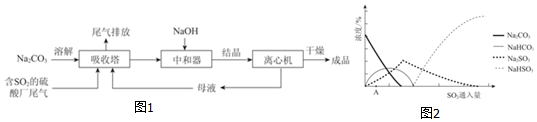
分析 Na2SO3应用广泛,利用工业废碱渣(主要成分Na2CO3)吸收硫酸厂尾气中的SO2制备无水Na2SO3,吸收塔中发生的反应为2CO32-+SO2+H2O=2HCO3-+SO32-,为了降低由中和器所得溶液中Na2SO3的溶解度,从而提高结晶产率,中和器中加入的NaOH是过量的,加入氢氧化钠进入中和器得到溶液结晶进入离心机干燥得到晶体,滤液重新进入吸收塔循环使用.
(1)二氧化硫在空气中变化生成硫酸,会导致酸雨;
(2)由图可知,初期反应(图中A点以前)碳酸钠与二氧化硫反应生成碳酸氢钠与亚硫酸钠;
(3)随着二氧化硫通入量增大,后期生成主要是得到亚硫酸氢钠,中和器中主要是将亚硫酸氢钠转化为硫酸钠,同时碳酸氢钠反应得到碳酸钠;
(4)①Na2SO3溶解电离出钠离子,NaOH过量使c(Na+)增大,抑制Na2SO3溶解;
②由于冷却至33℃以下时析出Na2SO3•7H2O,应在较高温度下蒸发浓缩至有大量晶体析出,利用余热蒸发;
(5)用盐酸除去亚硫酸钠,再用氯化钡溶液检验硫酸根离子;
(6)①IO3-与SO32-发生氧化还原反应得到SO42-与I-,I元素化合价降低6价,S元素化合价升高2价,化合价升降最小公倍数为6,可得IO3-的系数为1、SO32-的系数为3,再结合原子守恒、电荷守恒配平;
②根据离子方程式计算亚硫酸钠的物质的量,进而计算其质量分数.
解答 解:(1)向大气中排放SO2会导致酸雨发生,SO2气体在空气中经粉尘催化氧化为SO3,SO3与水反应能生成硫酸,有关反应的化学方程式为:2SO2+O2 $\frac{\underline{\;催化剂\;}}{\;}$2SO3;SO3+H2O═H2SO4,或二氧化硫与水反应生成亚硫酸,又被氧化为硫酸,则SO2形成硫酸型酸雨的反应为SO2+H2O?H2SO3、2H2SO3+O2═2H2SO4,
故答案为:酸雨;
(2)由图可知,初期反应(图中A点以前)碳酸钠与二氧化硫反应生成碳酸氢钠与亚硫酸钠,反应离子方程式为:2CO32-+SO2+H2O=2HCO3-+SO32-,
故答案为:2CO32-+SO2+H2O=2HCO3-+SO32-;
(3)随着二氧化硫通入量增大,后期生成主要是得到亚硫酸氢钠,中和器中主要是将亚硫酸氢钠转化为硫酸钠,同时碳酸氢钠反应得到碳酸钠,主要反应化学方程式为:NaHSO3+NaOH=Na2SO3+H2O,
故答案为:NaHSO3+NaOH=Na2SO3+H2O;
(4)①Na2SO3存在溶解平衡:Na2SO3(s)?2Na+ (aq)+SO32- (aq),NaOH过量使c(Na+)增大,上述平衡逆向移动,抑制Na2SO3溶解,
故答案为:Na2SO3存在溶解平衡:Na2SO3(s)?2Na+ (aq)+SO32- (aq),NaOH过量使c(Na+)增大,上述平衡逆向移动;
②a.加热蒸发直至蒸干,容易使固体溅出,导致损失等,故a错误
B.维持95~100℃蒸发浓缩至有大量晶体析出,再利用余热蒸干,故B正确;
C.由于冷却至33℃以下时析出Na2SO3•7H2O,应在较高温度下蒸发浓缩结晶,故C错误,
故答案为:b;
(5)用盐酸除去亚硫酸钠,防止干扰,再用氯化钡溶液检验硫酸根离子,
故答案为:稀盐酸、BaCl2溶液;
(6)①IO3-与SO32-发生氧化还原反应得到SO42-与I-,I元素化合价降低6价,S元素化合价升高2价,化合价升降最小公倍数为6,可得IO3-的系数为1、SO32-的系数为3,配平后离子方程式为:IO3-+3SO32-=3SO42-+I-,
故答案为:1、3、3SO42-、1I-;
②消耗KIO3的物质的量为y×10-3L×x mol/L=xy×10-3mol,
由IO3-+3SO32-=3SO42-+I-,可知n(Na2SO3)=3n(KIO3)=3xy×10-3mol
则成品中Na2SO3的质量分数为$\frac{3xy×1{0}^{-3}mol×126g/mol}{0.126g}$×100%=3xy×100%,
故答案为:3xy×100%.
点评 本题以物质制备为载体,考查学生对原理的分析理解、物质的分离提纯、氧化还原反应、物质含量测定、实验方案设计、信息获取与迁移运用等,需要学生具备扎实的基础,题目难度中等.


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃,pH=11的Na2CO3溶液中由水电离出的H+的数目为10-3NA | |
| B. | 标准状况下,2.24L NO与11.2L O2混合后气体的分子数小于NA | |
| C. | 120g熔融的NaHSO4中含阳离子总数为2NA | |
| D. | 用5mL 3mol/L FeCl3溶液制成的氢氧化铁胶体中所含胶粒数为0.015NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
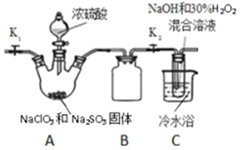 亚氯酸钠(NaClO2)和ClO2都是重要的漂白剂.通常情况下,ClO2是一种具有强氧化性的黄色气体,常用于水的净化和纸浆、纺织品的漂白.ClO2易发生爆炸,在生产、使用时可用其它气体进行稀释.ClO2易与碱反应生成亚氯酸盐和氯酸盐.
亚氯酸钠(NaClO2)和ClO2都是重要的漂白剂.通常情况下,ClO2是一种具有强氧化性的黄色气体,常用于水的净化和纸浆、纺织品的漂白.ClO2易发生爆炸,在生产、使用时可用其它气体进行稀释.ClO2易与碱反应生成亚氯酸盐和氯酸盐.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
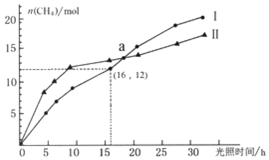 可利用如下反应将二氧化碳转化为甲烷:CO2(g)+2H2O(g)?CH4(g)+2O2(g)△H=+802KJ/mol,右图为在恒温、光照、不同初始浓度和不同催化剂(Ⅰ、Ⅱ)作用下,体积为2L的莫比容器中n(CH4)随光照时间的变化曲线.下列说法正确的是( )
可利用如下反应将二氧化碳转化为甲烷:CO2(g)+2H2O(g)?CH4(g)+2O2(g)△H=+802KJ/mol,右图为在恒温、光照、不同初始浓度和不同催化剂(Ⅰ、Ⅱ)作用下,体积为2L的莫比容器中n(CH4)随光照时间的变化曲线.下列说法正确的是( )| A. | 0-15h内,催化剂Ⅱ的催化效果比催化剂Ⅰ效果好 | |
| B. | 反应开始后的30h内,第Ⅰ种催化剂的作用下,反应吸收的热量多 | |
| C. | a点时,CO2的转化率相等 | |
| D. | 0-16h内,v(O2)=1.5mol/(L•h) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
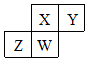 短周期元素X、Y、Z、W在元素周期表中的相对位置如表所示,W原子的质子数是其最外层电子数的三倍.下列说法不正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如表所示,W原子的质子数是其最外层电子数的三倍.下列说法不正确的是( )| A. | 元素Y有同素异形体 | |
| B. | 最高价氧化物对应水化物的酸性:X>Z | |
| C. | 简单气态氢化物的热稳定性:Y>Z | |
| D. | 原于半径:W>Z>Y>X |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该物质的分子式为SN | |
| B. | 该物质熔、沸点较低 | |
| C. | 该物质分子中所有原子的最外层均达到稳定结构 | |
| D. | 该物质与化合物S2N2互为同素异形体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向蛋白质溶液中加入浓氯化铁溶液 | |
| B. | 两种不同品牌的墨水混合 | |
| C. | 向饱和BaSO4溶液中加入浓BaCl2溶液 | |
| D. | 向饱和Na2CO3溶液中通入CO2气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com