
分子式为C10H14,属于苯的同系物,且苯环上的一氯代物只有2种的有机物有(不考虑立体异构,苯环上至少有3个氢)
A.5种 B.6种 C.7种 D.8种
科目:高中化学 来源: 题型:
正误判断,正确的打“√”,错误的打“×”
(1)所有的燃烧反应都是放热反应,所以不需要加热就能进行( )
(2)反应物的总能量低于生成物的总能量时,一定不能发生反应( )
(3)物理变化过程中,也可能有热量的变化( )
(4)C(石墨,s)===C(金刚石,s) ΔH>0,说明石墨比金刚石稳定( )
(5)一个反应的焓变因反应物的用量和反应条件的改变而发生改变( )
(6)催化剂能改变反应的焓变( )
(7)已知S(l)+O2(g)===SO2(g) ΔH=-293.23 kJ·mol-1,则S(s)+O2(g)===SO2(g)反应放出的热量大于293.23 kJ·mol-1( )
(8)同温同压下,H2(g)+Cl2(g)===2HCl(g),在光照和点燃条件下的ΔH不同( )
查看答案和解析>>
科目:高中化学 来源: 题型:
在氯化铁、氯化铜和盐酸的混合溶液中加入铁粉,待反应结束后,所剩余的固体滤出后能被磁铁吸引,反应后溶液存在较多的阳离子是 ( )
A.Cu2+ B.Fe3+ C.Fe2+ D.H+
查看答案和解析>>
科目:高中化学 来源: 题型:
某反应的反应过程中能量的变化如图所示,图中E1表示正反应的活化能,E2表示逆反应的活化能,下列有关叙述正确的是
A.该反应为放热反应
B.催化剂能改变该反应的焓变
C.E1也可表示反应物断键需要吸收的总能量 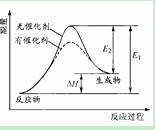
D.△H=E2-E1
查看答案和解析>>
科目:高中化学 来源: 题型:
对于常温下pH=11的氨水溶液,下列说法中正确的是
A.加水稀释100倍,9<pH<11
B.加入少量NH4Cl固体,溶液的pH升高
C.加水稀释后c(OH-)/c(NH3·H2O)值将减小
D.完全中和等浓度等体积的盐酸,耗氨水的体积比pH=11的NaOH溶液大
查看答案和解析>>
科目:高中化学 来源: 题型:
⑴已知反应Ⅰ:4NH3(g)+3O2(g)==2N2(g)+6H2O(g) △H=-1266.8kJ/mol
反应Ⅱ:N2(g) + O2(g)== 2NO(g) △=+180.5kJ/mol
它们的平衡常数依次为K1、K2
①写出氨高温催化氧化生成NO的热化学方程式 ,该反应的化学平衡常数的表达式K= (用含K1、K2的代数式表示)。
②反应Ⅰ可设计成燃料电池,若该电池以KOH溶液作电解质溶液,则负极的电极反应式为: 。该电池使用过程中,正极附近溶液的pH将 (填“升高”、“降低”或“不变”)。
⑵已知:N2(g) +3H2(g)  2NH3(g) △H=-92kJ/mol。
2NH3(g) △H=-92kJ/mol。
①为提高H2的转化率,宜采取的措施有 (填字母)
A.及时移出氨 B.升高温度 C.使用催化剂 D.循环利用和不断补充N2
②在一定温度、压强下,将N2和H2按体积比1:3在密闭容器中混合,当反应达平衡时,测得平衡混合气体中NH3的体积分数为25%,此时H2的转化率为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
水溶液中能大量共存的一组离子是( )
A.Na+、Ca2+、Cl-、SO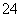
B.Fe2+、H+、SO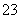 、ClO-
、ClO-
C.Mg2+、NH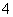 、Cl-、SO
、Cl-、SO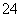
D.K+、Fe3+、NO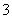 、SCN-
、SCN-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式书写正确的是( )
A.等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合:Ba2++2OH-+NH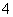 +HCO
+HCO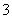 ===BaCO3↓+NH3·H2O+H2O
===BaCO3↓+NH3·H2O+H2O
B.实验室配制的亚铁盐溶液在空气中被氧化:4Fe2++O2+2H2O===4Fe3++4OH-
C.向碳酸氢铵溶液中加过量石灰水并加热:NH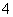 +OH-
+OH-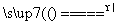 NH3↑+H2O
NH3↑+H2O
D.用酸化的高锰酸钾溶液氧化双氧水:2MnO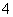 +6H++H2O2===2Mn2++3O2↑+4H2O
+6H++H2O2===2Mn2++3O2↑+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
20℃时,H2S的饱和溶液1 L,浓度约0.1 mol·L-1,其电离方程式为:第一步:H2S
 H++HS-;第二步:HS-
H++HS-;第二步:HS-
 H++S2-,若使溶液中H+、S2-浓度同时减小,可采取的措施是( )
H++S2-,若使溶液中H+、S2-浓度同时减小,可采取的措施是( )
①加入适量NaOH固体 ②加入适量水 ③通入适量SO2 ④加入适量CuSO4固体
A.①④ B.②④ C.②③ D.①③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com