
| A. | 4Fe(0H)2+O2+2H2O═4Fe(OH)3 | B. | 2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑ | ||
| C. | 3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$3CO2+2Fe | D. | Zn+H2SO4═ZnSO4+H2↑ |
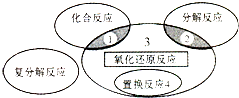
分析 区域3所表示的反应是氧化还原反应,但不是置换反应,不是化合反应,不是分解反应.据此分析.
解答 解:A、反应4Fe(0H)2+O2+2H2O═4Fe(OH)3是氧化还原反应,但同时又是化合反应,故A错误;
B、2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑是氧化还原反应,但同时又是分解反应,故B错误;
C、3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$3CO2+2Fe是氧化还原反应,但不是置换反应,也不是化合反应和分解反应,故属于区域3,故C正确;
D、Zn+H2SO4=ZnSO4+H2↑是氧化还原反应,但又是置换反应,故D错误.
故选C.
点评 本题考查学生四大基本反应类型和氧化还原反应之间的关系知识,可以根据所学知识进行回答,难度不大.


 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:选择题
| A. | H2SO4电离方程式H2SO4=2H++S6++4O2- | |
| B. | H2、D2、T2互为同位素 | |
| C. | 18g H2O含有的电子数为10NA | |
| D. | ${\;}_{62}^{144}$Sm与${\;}_{62}^{150}$Sm的核外电子数和中子数均为62 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 42% | B. | 60% | C. | 70% | D. | 80% |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 物质 | △H(kJ/mol) |
| CO(g) | -283.0 |
| CH4(g) | -890.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某溶液与NaOH 溶液共热,产生使湿润的红色石蕊试纸变蓝色的气体,说明原溶液中存在NH4+ | |
| B. | 某溶液中加入AgNO3 溶液时,产生白色沉淀,说明原溶液中一定存在Cl- | |
| C. | 某溶液中滴加BaCl2 溶液时,产生白色沉淀,说明原溶液中一定存在SO42- | |
| D. | 焰色反应中火焰显黄色,说明样品中存在钠元素,不存在钾元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 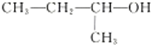 的名称为2-甲基-1-丙醇 的名称为2-甲基-1-丙醇 | |||||||||||||||||
| B. | 按照以下的排布规律,第15项物质可能与金属钠反应
| |||||||||||||||||
| C. | 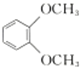 在核磁共振氢谱中出现两组峰,其氢原子个数之比为3:2 在核磁共振氢谱中出现两组峰,其氢原子个数之比为3:2 | |||||||||||||||||
| D. | 甲苯分子内所有原子均在同一平面 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com