
”¾ĢāÄæ”湤ŅµÉĻÖĘĮņĖįµÄÖ÷ŅŖ·“Ó¦Ö®Ņ»ĪŖ2SO2(g)+O2(g)![]() 2SO3(g)£¬·“Ó¦¹ż³ĢÖŠÄÜĮæµÄ±ä»ÆČēĶ¼ĖłŹ¾”£
2SO3(g)£¬·“Ó¦¹ż³ĢÖŠÄÜĮæµÄ±ä»ÆČēĶ¼ĖłŹ¾”£
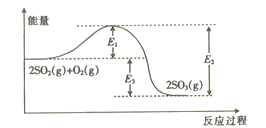
£Ø1£©ÓÉĶ¼æÉÖŖøĆ·“Ó¦µÄÕż·“Ó¦ĪŖ_____________(Ģī”°ĪüČČ”±»ņ”°·ÅČČ”±)·“Ó¦”£
£Ø2£©ÉżøßĪĀ¶Č£¬Ę½ŗāĻņ_________(Ģī”°Õż·“Ó¦”±»ņ”°Äę·“Ó¦”±)·½ĻņŅĘ¶Æ£»Õż·“Ó¦ĖŁĀŹ_____(Ģī”°Ōö“ó”±”°¼õŠ””±»ņ”°²»±ä”±£¬ĻĀĶ¬£©£¬Äę·“Ó¦ĖŁĀŹ_____________”£
£Ø3£©Ļņ·“Ó¦ĢåĻµÖŠ¼ÓČė“߻ƼĮŗó£¬Ķ¼ÖŠE1____(Ģī”°Ōö“ó”±”°¼õŠ””±»ņ”°²»±ä”±£¬ĻĀĶ¬£©£¬E3___________”£
£Ø4£©ŅŃÖŖ£ŗ2H2S(g)+O2(g)=2S(s)+2H2O(g) ”÷H=-442.4 kJ”¤mol-1£»
S(s)+O2(g)=SO2(g) ”÷H=-297.0 kJ mol-1”£
ŌņH2S(g)ÓėO2(g)·“Ó¦²śÉśSO2(g)ŗĶH2O(g)µÄČČ»Æѧ·½³ĢŹ½ŹĒ_________________£¬µ±“Ė·“Ó¦×ŖŅĘ3 molµē×ÓŹ±£¬·Å³öµÄČČĮæĪŖ_______kJ”£
”¾“š°ø”æ ·ÅČČ Äę·“Ó¦ Ōö“ó Ōö“ó ¼õŠ” ²»±ä 2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) ”÷H=-1036.4kJ”¤mol-1 259.1
”¾½āĪö”æ(1)·“Ó¦ÖŠ·“Ó¦ĪļµÄ×ÜÄÜĮæøßÓŚÉś³ÉĪļµÄ×ÜÄÜĮ棬¹Ź·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬¹Ź“š°øĪŖ£ŗ·ÅČČ£» (2) ÉżĪĀ£¬·ÅČČ·“Ó¦ÄęĻņŅĘ¶Æ£¬Õż·“Ó¦ŗĶÄę·“Ó¦ĖŁĀŹ¶¼Ōö“󣬹Ź“š°øĪŖ£ŗÄę·“Ó¦£»Ōö“ó£»Ōö“󣻣Ø3£©¼ÓČė“߻ƼĮ£¬æÉŅŌ½µµĶ·“Ó¦µÄ»ī»ÆÄÜE1£¬µ«·“Ó¦ČČE3²»±ä£¬¹Ź“š°øĪŖ£ŗ¼õŠ”£»²»±ä£»£Ø4£©øł¾ŻøĒĖ¹¶ØĀÉ·ÖĪö£¬¢Ł2H2S(g)+O2(g)=2S(s)+2H2O(g) ”÷H=-442.4 kJ”¤mol-1£»
¢ŚS(s)+O2(g)=SO2(g) ”÷H=-297.0 kJ mol-1£¬ÓÉ¢Ł+¢Ś”Į2¼“æɵĆČČ»Æѧ·½³ĢŹ½ĪŖ2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) ”÷H=-442.4-297.0”Į2=-1036.4kJ”¤mol-1£»øĆ·“Ó¦ÖŠ×ŖŅĘ12Ħ¶ūµē×Ó£¬ĖłŅŌµ±×ŖŅĘ3Ħ¶ūµē×ÓŹ±·Å³öµÄČČĮæĪŖ1036.4/4= 259.1 kJ£¬¹Ź“š°øĪŖ£ŗ2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) ”÷H=-1036.4kJ”¤mol-1 £» 259.1”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻņŗ¬Fe2+”¢I©”¢Br©µÄČÜŅŗÖŠĶØČė¹żĮæµÄĀČĘų£¬ČÜŅŗÖŠĖÄÖÖĮ£×ÓµÄĪļÖŹµÄĮæ±ä»ÆČēĶ¼ĖłŹ¾£¬ŅŃÖŖb©a=5£¬Ļ߶Ī¢ō±ķŹ¾Ņ»ÖÖŗ¬ŃõĖį£¬ĒŅ¢ńŗĶ¢ō±ķŹ¾µÄĪļÖŹÖŠŗ¬ÓŠĻąĶ¬µÄŌŖĖŲ£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©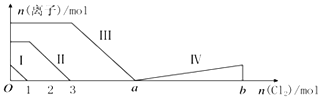
A.Ļ߶Ī¢ņ±ķŹ¾Br©µÄ±ä»ÆĒéæö
B.Ļ߶Ī¢ō±ķŹ¾IO3©µÄ±ä»ÆĒéæö£¬ĘäÖŠIO3©Ōö¼ÓĮĖ5moL£®
C.a=6
D.ŌČÜŅŗÖŠn£ØFeI2£©£ŗn£ØFeBr2£©=3£ŗ1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĖłĪ½ŗĻ½š£¬¾ĶŹĒ²»Ķ¬ÖÖ½šŹō(Ņ²°üĄØŅ»Š©·Ē½šŹō)ŌŚČŪ»ÆדĢ¬ĻĀŠĪ³ÉµÄŅ»ÖÖČŪŗĻĪļ£¬ĻĀ±ķĪŖĖÄÖÖ½šŹōµÄČŪ”¢·Šµć£ŗ
Na | Cu | Al | Fe | |
ČŪµć/”ę | 97.5 | 1083 | 660 | 1535 |
·Šµć/”ę | 883 | 2595 | 2200 | 3000 |
øł¾ŻŅŌÉĻŹż¾ŻÅŠ¶ĻĘäÖŠ²»ÄÜŠĪ³ÉŗĻ½šµÄŹĒ(””””)
A. CuŗĶNaB. FeŗĶCu
C. FeŗĶAlD. AlŗĶNa
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ
A.ŹµŃéŹŅÓĆ¼ÓČČNH4Cl¹ĢĢåµÄ·½·ØÖʱøNH3
B.ÓƵćČ¼µÄ»š²ńŌŚŅŗ»ÆĘųøÖĘææŚ¼ģŃéŹĒ·ńĀ©Ęų
C.¹¤ŅµÉĻÓĆSO2ĘÆ°×Ö½½¬”¢Ć«”¢Ė攢²ŻĆ±±čµČ
D.±£“ę½šŹōÄĘµÄ²Öæā×Å»šæÉŅŌÓƶžŃõ»ÆĢ¼Ćš»šĘ÷Č„Ćš»š
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¼ČæÉŅŌÓĆĄ“¼ų±š¼×ĶéŗĶŅŅĻ©£¬ÓÖæÉŅŌÓĆĄ“³żČ„¼×ĶéÖŠ»ģÓŠµÄÉŁĮæŅŅĻ©µÄŹĒ
A. ĘųĢåĶعżŹ¢ÓŠĖįŠŌøßĆĢĖį¼ŲČÜŅŗµÄĻ“ĘųĘæ
B. ĘųĢåĶعżŹ¢ÓŠ×ćĮæäåĖ®µÄĻ“ĘųĘæ
C. ĘųĢåĶعżŹ¢ÓŠ×ćĮæÕōĮóĖ®µÄĻ“ĘųĘæ
D. ĘųĢåÓėŹŹĮæHC1»ģŗĻ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹÖŠŹōÓŚµē½āÖŹµÄŹĒ
A. ŅŅ“¼ B. CO2 C. ÉÕ¼ī D. ½šŹōĢś
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ·Ö×ÓŹ½ĪŖC4H9ClµÄĶ¬·ÖŅģ¹¹ĢåÓŠ£Ø £©
A.1ÖÖ
B.2ÖÖ
C.3ÖÖ
D.4ÖÖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĦ¶ūŃĪ[£ØNH4£©2Fe£ØSO4£©26H2O]ŹĒ·ÖĪö»Æѧ֊µÄÖŲŅŖŹŌ¼Į£®Ä¦¶ūŃĪøō¾ųæÕĘų¼ÓČČæÉĶźČ«·Ö½āÉś³Éŗģ×ŲÉ«¹ĢĢåŗĶĘäĖū²śĪļ£®Ä³Ń§Ļ°Š”×éÓūĢ½¾æĘä·Ö½ā²śĪļ£®
£Ø1£©¼××éĶ¬Ń§Éč¼ĘĮĖČēĶ¼1ĖłŹ¾ŹµŃé×°ÖĆ£® 
£Øi£©ŹµŃéÖŠ£¬×°ÖĆBÖŠ¹Ū²ģµ½µÄĻÖĻóŹĒ £®
£Øii£©¼īŹÆ»ŅµÄÖ÷ŅŖ×÷ÓĆŹĒ £®
£Øiii£©×°ÖĆDÖŠ¹Ū²ģµ½·ÓĢŖČÜŅŗ±äŗģÉ«£¬ÓÉ“ĖæÉÖŖĦ¶ūŃĪ·Ö½āµÄ²śĪļÖŠÓŠ£ØŠ“»ÆѧŹ½£©£®
£Øiv£©Éč¼ĘŹµŃéŃé֤װÖĆAÖŠ¹ĢĢ岊ĮōĪļ²»ŗ¬FeO£ŗ£Ø¼ņŅŖĖµĆ÷ŹµŃé²Ł×÷”¢ĻÖĻóŗĶ½įĀŪ£©£®
£Ø2£©ŅŅ×éĶ¬Ń§ČĻĪŖĦ¶ūŃĪŹÜČČ·Ö½āµÄ²śĪļÖŠ»¹ŗ¬ÓŠSO2”¢SO3ŗĶN2 £® ĪŖ½ųŠŠŃéÖ¤£¬ÓĆ¼××鏵ŃéÖŠµÄ×°ÖĆAŗĶĻĀĮŠČēĶ¼2ĖłŹ¾×°ÖĆ½ųŠŠŹµŃ飮
ĖµĆ÷“Ė¹ĢĢå²śĪļ²»ŗ¬FeO|¶ąÓą
£Øi£©ŅŅ×éĶ¬Ń§µÄŹµŃé×°ÖĆÖŠ£¬ŅĄ“ĪĮ¬½ÓµÄŗĻĄķĖ³ŠņĪŖA”¢ £® ×°ÖĆGÖŠŃĪĖįµÄ×÷ÓĆŹĒ
£Øii£©ŹµŃéÖŠ£¬×¼Č·³ĘĮæĦ¶ūŃĪ7.8400g£¬³ä·Ö¼ÓČČ·“Ó¦ŗ󣬲āµĆ×°ÖĆAÖŠ¹ĢĢ岊ĮōĪļµÄÖŹĮæĪŖ1.6000g£¬×°ÖĆGÖŠÉś³É°×É«³ĮµķµÄÖŹĮæĪŖ3.4950g£¬×°ÖĆHÖŠŹÕ¼Æµ½112mL N2£Ø±ź×¼×“æöĻĀ£©£¬Š“³öĦ¶ūŃĪŹÜČČ·Ö½āµÄ»Æѧ·½³ĢŹ½£ŗ £® £Ø·Ö½ā²śĪļ±»³ä·ÖĪüŹÕ£¬²»æ¼ĀĒĘäĖšŹ§£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»ÖÖ¹ā»Æѧµē³ŲµÄ½į¹¹ČēĶ¼ĖłŹ¾£¬µē³Ų×Ü·“Ó¦ĪŖ£ŗAgCl(s)£«Cu£«(aq)===Ag(s)£«Cu2£«(aq)£«Cl£(aq)£¬ĻĀĮŠ¹ŲÓŚøƵē³ŲŌŚ¹¤×÷Ź±µÄĖµ·ØÖŠÕżČ·µÄŹĒ

A. Éś³É108 gŅų£¬×ŖŅʵē×ÓøöŹżĪŖ1 mol
B. Cu£«ŌŚøŗ¼«·¢ÉśŃõ»Æ·“Ó¦
C. Agµē¼«»īĘĆ£¬AgŹ§µē×Ó·¢ÉśŃõ»Æ·“Ó¦
D. Cl£ÓÉøŗ¼«ĒØŅʵ½Õż¼«
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com