
 氢能是一种极具发展潜力的清洁能源.硫碘循环分解水是最具潜力的制氢方法.其反应原理如下:
氢能是一种极具发展潜力的清洁能源.硫碘循环分解水是最具潜力的制氢方法.其反应原理如下:分析 (1)反应Ⅱ为分解反应,应在加热条件下进行;
①a.硫酸和HI溶液不分层;
b.由题给信息可知溶液的密度与碘的浓度有关;
c.由题给信息可知碘在HI溶液中浓度较大.
②可观察溶液的颜色判断;
(2)已知:①SO3(g)+H2O(g)=H2SO4(l)△H=-177kJ/mol,②2SO3(g)=2SO2(g)+O2(g)△H=+196kJ/mol,利用盖斯定理将②-①×2可得2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g)的△H;
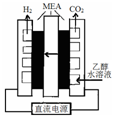
(3)①阴极发生还原反应生成氢气,应先排出空气;
②由图示可知乙醇被氧化生成二氧化碳.
解答 解:(1)反应Ⅱ的△S>0,如能自发进行,应满足△H-T•△S∵0,在低温条件下不能自发进行,说明△H>0,故答案为:△H>0;
①a.硫酸和HI都溶于水,溶液不分层,故a错误;
b.由题给信息可知溶液的密度与碘的浓度有关,不能确定碘的HI以及硫酸溶液的密度大小,故b错误;
c.由题给信息可知碘在HI溶液中浓度较大,故c正确.
故答案为:c;
②由题给信息可知混合物分成两层--上层是含低浓度I2的H2SO4层和下层是高浓度的I2的HI层,可观察颜色,颜色深的是HI层,颜色浅的是硫酸层,
故答案为:观察颜色,颜色深的是HI层,颜色浅的是硫酸层;
③溶液中存在电荷守恒c(H+)=c(OH-)+c(I-)+c(I3-),则c(H+) 大于c(I-)+c(I3-),故答案为:大于;
(2)已知:①SO3(g)+H2O(g)=H2SO4(l)△H=-177kJ/mol,②2SO3(g)=2SO2(g)+O2(g)△H=+196kJ/mol,
利用盖斯定理将②-①×2可得2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g)的△H=196kJ/mol-2×(-177kJ/mol)=+550kJ/mol,
故答案为:+550;
(3)①阴极发生还原反应生成氢气,应先排出空气,可通入氩气,故答案为:赶出装置中的空气;
②由图示可知乙醇被氧化生成二氧化碳,电极方程式为 CH3CH2OH+3H2O-12e-=2CO2↑+12H+,故答案为:CH3CH2OH+3H2O-12e-=2CO2↑+12H+.
点评 本题考查较为综合,化学反应与能量变化、离子浓度大小比较以及原电池知识,为高频考点,侧重于学生的分析能力和计算能力的考查,难度中等.


 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源: 题型:解答题
| 温度 | 25℃~550℃~600℃~700℃ |
| 主要成分 | WO3 W2O5 WO2 W |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 性质 | 实际应用 |
| A | MgO熔点高 | 可用作耐火材料 |
| B | KMnO4具有强氧化性 | 可用于漂白织物 |
| C | 常温下,铁能被浓硫酸钝化 | 常温下,可用铁质器皿盛放浓硫酸 |
| D | TiCl4在水中能发生水解 | 可用TiCl4溶液制备TiO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液氨汽化时要吸收大量的热,可用作制冷剂 | |
| B. | 次氯酸钠具有碱性,可用于配制“84”消毒液 | |
| C. | Al2O3具有很高的熔点,可用于制造熔融烧碱的坩埚 | |
| D. | SiO2既能溶于NaOH溶液又能溶于HF溶液,说明SiO2是两性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 向浓度为0.1mol•L-1的NaHCO3溶液中滴加少量盐酸后所得溶液中:c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| B. | pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合所得溶液中:c(CH3COO-)+c(H+)>c(Na+)+c(OH-) | |
| C. | 0.1 mol•L-1CH3COOH溶液和0.1 mol•L-1CH3COONa溶液等体积混合:c(Na+)>c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) | |
| D. | 0.1 mol•L-1 NH4HSO4溶液中滴加0.1 mol•L-1 NaOH溶液至中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiC是氧化产物 | |
| B. | 还原剂与氧化剂的物质的量之比为1:2 | |
| C. | 若生成4.48LCO,则转移0.4 mol 电子 | |
| D. | C 既是氧化剂又是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 物质 | 杂质 | 试剂或用品 | 主要操作 | |
| A | 淀粉 | 碘化钾 | 半透膜 | 渗析 |
| B | Fe(NO3)2 | Ba(NO3)2 | 硫酸 | 过滤 |
| C | Fe | I2 | / | 加热 |
| D | 溴 | 四氧化碳 | 蒸馏装置 | 蒸馏 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
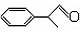 )曾入选伦敦奥运会指定产品,下面是工业合成龙葵醛的路线图(部分反应条件及副产物已略去),回答问题:
)曾入选伦敦奥运会指定产品,下面是工业合成龙葵醛的路线图(部分反应条件及副产物已略去),回答问题: $→_{催化剂}^{CH_{3}CH=CH_{2}}$$\stackrel{A}{{C}_{9}{H}_{12}}$$→_{光照}^{Cl_{2}}$$\stackrel{B}{{C}_{9}{H}_{11}{C}_{1}}$→${\stackrel{C}{{C}_{9}{H}_{10}}}_{\;}$$\stackrel{HBr}{→}$$\stackrel{D}{{C}_{9}{H}_{11}Br}$→$\stackrel{E}{{C}_{9}{H}_{12}O}$$→_{△}^{催化剂}$龙葵醛
$→_{催化剂}^{CH_{3}CH=CH_{2}}$$\stackrel{A}{{C}_{9}{H}_{12}}$$→_{光照}^{Cl_{2}}$$\stackrel{B}{{C}_{9}{H}_{11}{C}_{1}}$→${\stackrel{C}{{C}_{9}{H}_{10}}}_{\;}$$\stackrel{HBr}{→}$$\stackrel{D}{{C}_{9}{H}_{11}Br}$→$\stackrel{E}{{C}_{9}{H}_{12}O}$$→_{△}^{催化剂}$龙葵醛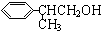 +O2
+O2
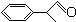 +2H2O.
+2H2O. 或
或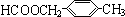 (任写一种).
(任写一种).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生活污水使用明矾杀菌消毒 | B. | 向燃煤中加入适量石灰石“固硫” | ||
| C. | 推广使用可降解塑料防止白色污染 | D. | 提倡公交出行可减少氮氧化物排放 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com