
| A. | HSO3-+H20?SO32-+H3O+ | B. | S2-+H2O?H2S+2OH- | ||
| C. | Cu2++4H2O?Cu(OH)2+2H3O+ | D. | NH3•H2O+H3O+?NH4++2H2O |
分析 盐类水解是含弱离子的盐溶液中结合水电离出的氢离子或氢氧根离子,促进水电离平衡正向进行,导致溶液中氢离子浓度和氢氧根离子浓度不同,溶液显示了酸碱性,水解过程是酸碱中和反应的逆反应,反应过程微弱,离子方程式用可逆号,多元弱酸分步水解;
A.离子方程式为电离方程式;
B.多元弱酸阴离子分步水解;
C.铜离子结合水电离出的氢氧根离子生成氢氧化铜,促进水的电离;
D.离子方程式是一水合氨和酸反应生成铵盐的化学反应.
解答 解:A.选项中离子方程式为电离方程式,水解离子方程式应为:HSO3-+H20?H2SO3+OH-,故A错误;
B.多元弱酸阴离子分步水解,离子方程式应为;S2-+H2O?HS-+OH-,故B错误;
C.铜离子结合水电离出的氢氧根离子生成氢氧化铜,促进水的电离,Cu2++4H2O?Cu(OH)2+2H3O+,氢离子写成水合氢离子,离子方程式是水解离子方程式,故C正确;
D.离子方程式是一水合氨和酸反应生成铵盐的化学反应,NH3•H2O+H3O+?NH4++2H2O,氢离子写成水合氢离子,即为NH3•H2O+H+?NH4++H2O,故D错误;
故选C.
点评 本题考查了盐类水解的原理,离子方程式书写方法,注意氢离子的书写方法,多元弱酸阴离子分步水解,题目难度中等.


 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:高中化学 来源: 题型:选择题
| A. | 除去N2中的少量O2:通过灼热的Cu粉,收集气体 | |
| B. | 除去Cl2中的少量HCl:通入饱和NaCl溶液,干燥后收集气体 | |
| C. | 除去Fe2O3固体中少量Al2O3:加入足量NaOH溶液,过滤、洗涤、干燥 | |
| D. | 除去Na2CO3溶液中的NaHCO3可采用加热的方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
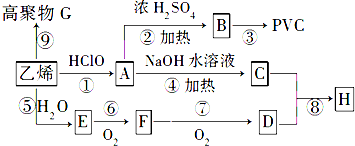
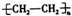 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
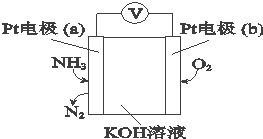
| A. | O2在电极b上发生还原反应 | |
| B. | 溶液中OH-向电极a移动 | |
| C. | 反应消耗的NH3与O2的物质的量之比为3:4 | |
| D. | 负极的电极反应式为:2NH3-6e-+6OH-═N2+6H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 电极材料 | Cu、Zn | Cu、Ag | Fe、Zn | Cu、C |
| 插入溶液 | FeCl3 | Fe(NO3) 2 | CuSO4 | Fe2(SO4)3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钢是用量最大的合金 | |
| B. | 铝锂合金抗腐蚀能力很强,可耐酸碱腐蚀 | |
| C. | 我国在商代就开始使用铜合金 | |
| D. | 铝合金的强度、硬度比纯铝大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
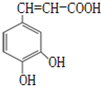
| A. | 分子式为C9H8O4 | |
| B. | 1mol咖啡酸最多能与4mol氢气发生加成反应 | |
| C. | 遇溴水,既能发生取代反应又能发生加成反应 | |
| D. | 能还原酸性KMnO4溶液,说明其分子中含有碳碳双键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 偏铝酸钡 Ba(AlO2)2 | B. | 明矾 KAl(SO4)2•12H2O | ||
| C. | 醋酸钙 (CH3COO)2Ca | D. | 亚硫酸氢钙 CaHSO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Z、W、Q三种元素的单质属于三种不同的晶体类型 | |
| B. | Q氢化物的熔点高于Z氢化物的熔点 | |
| C. | 一定条件下,Q单质可把Y从其氢化物中置换出来 | |
| D. | 最高价氧化物对应水化物的酸性顺序:Q>Y>W>X |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com