
| A. | 乙烷 | B. | 异丁烷 | C. | 异戊烷 | D. | 2,3-二甲基戊烷 |
分析 炔烃含有C≡C键,与氢气加成可生成C=C或-CH2-CH2-,结合碳原子只能形成4个共价键,故由炔烃加成而得到的产物中相邻的两个碳上应至少都有2个氢原子.
解答 解:A、乙烷CH3CH3中相邻的两个碳原子上均含3个H原子,故可以由炔烃加成而来,故A错误;
B、异丁烷(CH3)3CH中任何两个相邻的碳原子上均不含2个H原子,故不能由炔烃加成而来,故B正确;
C、异戊烷(CH3)2CHCH2CH3中3号和4号碳原子上分别至少含2个H原子,故可以由炔烃加成而来,故C错误;
D、2,3-二甲基戊烷中4号和5号碳原子上均至少含2个H原子,故可以由炔烃加成而来,故D错误.
故选B.
点评 本题考查有机物的结构和性质,侧重于学生的分析能力的考查,注意把握炔烃的性质以及碳原子的成键特点,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:实验题
| 实验 序号 | 反应温度 (℃) | 参加反应的物质 | ||||
| Na2S2O3 | H2SO4 | H2O | ||||
| V/mL | c/mol•L-1 | V/mL | c/mol•L-1 | V/mL | ||
| A | 20 | 10 | 0.1 | 10 | 0.1 | 0 |
| B | 20 | 5 | 0.1 | 10 | 0.1 | 5 |
| C | 20 | 10 | 0.1 | 5 | 0.1 | 5 |
| D | 40 | 5 | 0.1 | 10 | 0.1 | 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡是放热反应都是自发的,凡是吸热反应都是非自发的 | |
| B. | 自发反应一定是放热反应,非自发反应一定是吸热反应 | |
| C. | 自发反应在恰当条件下才能实现 | |
| D. | 自发反应在任何条件下都能实现 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
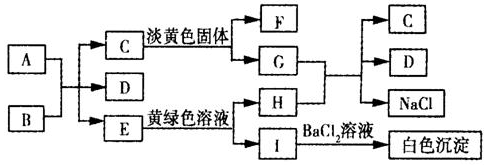
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
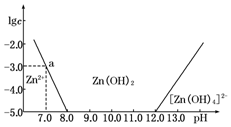
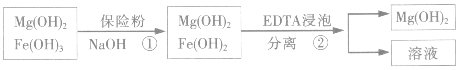
| 精制阻燃剂的条件 | 阻燃剂铁含量 | |||
| 序号 | 提纯体系温度/℃ | 加入EDTA质量/g | 加入保险粉质量/g | W(Fe)/(10-4g) |
| 1 | 40 | 0.05 | 0.05 | 7.63 |
| 2 | 40 | 0.05 | 0.10 | 6.83 |
| 3 | 60 | 0.05 | 0.10 | 6.83 |
| 4 | 60 | 0.10 | 0.10 | 6.51 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
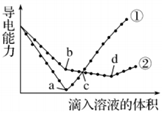
| A. | b点,水电离产生的c(H+)<10-7mol/L | B. | ①代表滴加H2SO4溶液的变化曲线 | ||
| C. | a、d两点对应的溶液均显中性 | D. | c点,两溶液中含有相同量的 OH- |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省高二上10月月考化学试卷(解析版) 题型:选择题
0.1mol/L NH4Cl溶液中,下列叙述错误的是 ( )
A.c(NH4+)>c(Cl—)>c(OH—)>c(H+)
B.c(Cl—)>c(NH4+)>c(H+)>c(OH—)
C.c(NH4+)+c(H+)=c(Cl—)+c(OH—)
D.c(NH4+)+c(NH3 ·H2O)=c(Cl—)
·H2O)=c(Cl—)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com