
【题目】下列试剂中不能用于鉴别乙醇和乙酸的是( )
A.金属NaB.酸性KMnO4溶液C.溴水D.NaHCO3溶液
科目:高中化学 来源: 题型:
【题目】已知某离子晶体晶胞如图所示,其摩尔质量为M,阿伏加德罗常数为NA,晶体的密度为d g/cm3。下列说法中正确的是( )

A. 晶体晶胞中阴、阳离子的个数都为1
B. 其中阴、阳离子的配位数都是4
C. 该晶胞可能是NaCl的晶胞
D. 该晶体中两个距离最近的阳离子的核间距为![]() cm
cm
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以砷烟灰(主要含PbO、As2S3、In2O2、In2S3等) 为原料回收稀散金属铟(In)。铟是稀缺资源,主要应用于在透明导电涂层、荧光材料、有机合成等,铟的逆流氧化酸浸工艺流程及工艺条件如下:
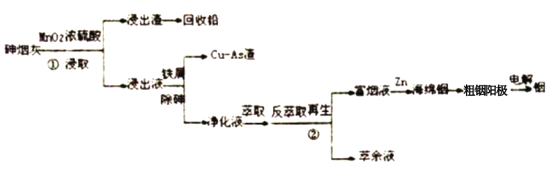
砷烟灰的逆流氧化酸浸工艺条件
项目 | 液固比 | 始酸酸度(g·L-l) | 终酸酸度(g·L-l) | 温度(℃) | 时间(h) | 锰粉加入量(%) |
一次浸出 | 3~7:1 | 90-120 | 30-80 | >95 | >4 | 3~7 |
二次浸出 | 3~7:1 | 150-180 | 120-150 | >95 | >4 | 10-15 |
(1) 流程中要多次进行混合物的分离,其中操作①的分离方法分别为_________,②的分离方法在实验室中使用的主要仪器为_________ 。
(2)下列有关流程说法不正确的是_________。
A.两次浸取时温度越高,浸出时间越长,工业效益越好
B.浸取时采用适宜的液固比,既可为下步萃取提供合适的酸度,又能得到较高浓度的In3+溶液
C.净化液通过萃取、反萃取、再生等过程可富集得到高浓度In3+溶液并使萃取剂循环利用
D.电解粗铟时阳极泥成分包括锌、铜、银等金属
(3)萃取净化液所用苯取剂可用H2A2表示,使In3+进入有机相,相关反应可表示为: In3++3H2A2![]() In (HA2)3+3H+, 则反萃取所用试剂应选用_______(选 填:“ 稀硫酸”或“NaOH溶液”)
In (HA2)3+3H+, 则反萃取所用试剂应选用_______(选 填:“ 稀硫酸”或“NaOH溶液”)
(4)砷烟灰中的As2S3不溶于稀硫酸,但加入MnO2后可溶解,并转化为AsO43-,同时产生臭鸡蛋气味气体。该反应的化学方程式为______________。
(5)电解精炼粗铟时阴极材料应选用________,随着电解的不断进行,电解液中c(In3+)会逐渐________(填:“增大”、“减小”或“不变”)。
(6)工业上常采用ITO靶材废料回收铟,其浸出液中主要含Sn4+杂质,除杂可采用加入Na2S溶液的方法。要使Sn4+沉淀完全即c(Sn4+)低于10-5mol/L,
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E都是元素周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。B原子的p轨道半充满,形成的氢化物的沸点是同主族元素的氢化物中最低的。D原子得到一个电子后3p轨道全充满。A+比D原子形成的离子少一个电子层。C与A形成A2C型离子化合物。E的原子序数为26,E原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C、D的电负性由小到大的顺序为________________。
(2)C的最高价氧化物分子是________(填“极性”或“非极性”)分子。
(3)与B同主族元素X,其气态氢化物是同主族元素的氢化物中沸点最高的,解释X的气态氢化物极易溶于水的原因:①_______________②_______________
(4)E的一种常见配合物E(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂。据此可判断E(CO)5的晶体类型为____;E(CO)5在一定条件下发生分解反应:E(CO)5===E(s)+5CO,反应过程中,断裂的化学键只有配位键,形成的化学键是________________。
(5)金属E单质的晶体在不同温度下有两种堆积方式,晶胞如图所示。
体心立方晶胞和面心立方晶胞中E原子的配位数之比为________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对化学反应的速率和限度的叙述正确的是( )
A.增加某一反应物的用量一定能够加快该反应的速率
B.化学反应的限度是不可改变的
C.化学反应进行的时间越长该反应的限度越大
D.化学反应达到限度时,正逆反应速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】储氢纳米碳管的研究成功体现了科技的进步,但用电弧法合成的碳纳米管常伴有大量的杂质——碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯。其反应式为:3C+2K2Cr2O7 +8H2SO4===3CO2↑+2K2SO4
+2Cr2(SO4)3 +8H2O。
(1)请用双线桥法标出电子转移方向和数目________________________________。
(2)上述反应中氧化剂是______(填化学式),被氧化的元素是________(填元素符号)。
(3)H2SO4 在上述反应中表现出来的性质是____________(填序号)。
A.氧化性 B.氧化性和酸性 C.酸性 D.还原性和酸性
(4)若反应中电子转移了0.8 mol,则产生的气体在标准状况下的体积为_________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是一种化学性质很活泼的非金属单质,它具有较强的氧化性。下列叙述中不正确的是:
A. 红热的铜丝在氯气中剧烈燃烧,生成棕黄色烟
B. 钠在氯气中燃烧,生成白色的烟
C. 纯净的氢气在氯气中安静的燃烧,在集气瓶口形成白色烟雾
D. 氯气能与水反应生成盐酸和次氯酸,次氯酸见光易分解
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com