
| A. | 3种溶液pH的大小顺序是③>②>① | |
| B. | 若将3种溶液稀释相同倍数,pH变化最大的是② | |
| C. | 若分别加入25 mL 0.1 mol/L盐酸后,pH最大的是① | |
| D. | 3种溶液中,由水产生的c(H+)大小顺序是①>③>② |
分析 A.等浓度时强碱的pH最大;强碱弱酸盐中对应的酸酸性越强,水解程度越小,酸性越强,pH越小;
B.稀释时强碱的变化程度大;
C.根据酸碱混合后溶液中的溶质来分析;
D.碳酸钠和醋酸钠水解促进水的电离,氢氧化钠溶液是强碱抑制水的电离.
解答 解:A.等浓度时强碱的pH最大,强碱弱酸盐中对应的酸性越强,水解程度越小,碳酸氢根离子的酸性小于醋酸,所以3种溶液pH的大小顺序是③>①>②,故A错误;
B.稀释时强碱的变化程度大,所以三种溶液稀释相同倍数,pH变化最大的是③,故B错误;
C.等体积等浓度混合后,①中溶质为NaHCO3、NaCl,②中溶质为NaCl、CH3COOH,③中溶质为NaCl,而HCO3-离子水解显碱性,所以pH最大的是①,故C正确;
D.碳酸钠和醋酸钠水解促进水的电离,水解程度越大,对水的电离的促进程度越大,氢氧化钠溶液是强碱抑制水的电离,所以水产生的c(H+)大小顺序是①>②>③,故D错误;
故选:C.
点评 本题考查盐类水解、pH的判断等,明确酸碱混合的计算,盐类水解的规律、pH与浓度的关系等知识即可解答,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 碳酸钙溶于稀盐酸中:CO32-+2H+═H2O+CO2↑ | |
| B. | 氯化钡溶液与稀硫酸反应:Ba2++SO42-═BaSO4↓ | |
| C. | 铁与稀盐酸反应:2Fe+6H+═3H2↑+2Fe3+ | |
| D. | 铜片插入硝酸银溶液中:Cu+Ag+═Cu2++Ag |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应物能量总和大于生成物能量总和 | |
| B. | 反应中生成1mol水蒸气放出285.8 kJ的热量 | |
| C. | 2H2O(1)=2H2(g)+O2(g)△H=+571.6 kJ.mol-1 | |
| D. | 当反应中有2 mol H-H键断裂,该反应放出571.6 kJ的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯水的颜色呈浅黄绿色,是因为氯水中含有Cl2 | |
| B. | 新制氯水能使红色布条褪色,说明氯水中含HClO | |
| C. | 向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+ | |
| D. | 活性炭和氯水都具有漂白作用,且漂白的化学原理相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高纯度的硅单质用于制作光导纤维 | |
| B. | Al2O3熔点很高,可用作耐火材料 | |
| C. | SO2可以用来漂白面条 | |
| D. | N2与O2在放电条件下直接化合生成NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 用途 | 解释 |
| A | 可用FeCl3溶液刻蚀铜制电路板 | Fe3+的氧化性强于Cu2+ |
| B | 碳与石英反应可冶炼粗硅 | 碳的非金属性比硅强 |
| C | 四氯化碳可用于灭火 | 四氯化碳的沸点高 |
| D | 酸性KMnO4溶 液可漂白织物 | KMnO4有强氧化性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,11.2L氯气所含原子数目为NA | |
| B. | 3mol单质Fe完全转变为Fe3O4,失去8NA个电子 | |
| C. | 标准状况下,11.2L SO3 中含有2NA个原子 | |
| D. | 用石灰乳完全吸收1 mol Cl2时,转移电子的数目是2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
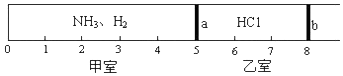
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com