
某同学利用如图装置制NO并进行相关实验探究。

(1)写出制备NO的反应方程式????????????????????????????????????? ?
(2)收集的气体与空气混合后变红色,这说明NO具有_____性。?
(3)制备NO的步骤如下:?
1按图所示连接好装置;
2取下注射器,通过U型长管加入稀硝酸至接近U型短管的铜丝?
3在针头上安装好注射器,抽出U型短管中的所有空气;然后拔出注射器,并排尽注射器中的空气。?
4待硝酸与铜丝分离后,用已排除空气的注射器抽出生成NO,将注射器针头插入橡皮塞中以封口。?
在上述操作中遗漏的一个步骤是???????????? ,在步骤3中可以观察到的现象为????????????????????? 。?????????????????????????
(4)在铜丝上绑上石墨的作用是????????????????????????????????? 。
(5)若将稀硝酸换成浓硝酸,则可制取NO2气体。请你用注射器收集NO2气体并完成“外界因素对化学平衡移动影响”实验探究,相关内容填在下面表格。(只完成一个影响因素的探究,其他实验用品自选)已知
2NO2(g)  N2O4(g) △H <0;N2O4为无色气体。?
N2O4(g) △H <0;N2O4为无色气体。?
实验步骤 | 实验现象 | 实验结论 |
①分别用两支注射器收集NO2,并将注射器针头插入橡皮塞中以封口。 ②_____________________ _______________________ ________________________ _______________________ ________________________ | _______________________ ________________________ _______________________ ________________________ _______________________ _______________________ ________________________ _______________________ | _______________________ ________________________ _______________________ ________________________ _______________________ _______________________ ________________________ _______________________ |
(1)3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O(2分)?
(2)还原 (2分)?
(3)检查装置的气密性(2分);u型管短管中溶液与铜丝接触反应;有气泡产生,溶液变蓝色,铜丝减少(2分)?
(4)形成原电池,加快反应速率(2分)?
(5)方案一:?
实验步骤? | 实验现象? | 实验结论? |
②将二支注射器分别插入装有热水、冰水的烧杯中(1分);几分钟后拿出作对比。(1分)? | 浸入热水的注射器中的气体颜色变深;(1分)? 浸入冰水的注射器中的气体颜色变浅。(1分)? | 在其他条件不变的情况下(1分),温度升高,会使化学平衡向着吸热反应的方向移动;温度降低会使化学平衡向放热反应的方向移动(1分)(只答一方面也给1分)? |
或:方案二:?
实验步骤? | 实验现象? | 实验结论? |
②将一支注射器的活塞迅速往里推到一定位置,然后与另一支注射器的气体作对比(1分);回复原状后再将注射器的活塞迅速往外拉到一定位置,然后与另一支注射器的气体作对比(1分)? | 迅速推动注射器,针管内气体颜色先变深后慢慢变浅(1分);迅速拉伸注射器时,针管内气体颜色先变浅后深慢慢变深。(1分)? | 在其他条件不变的情况下(1分),增大压强,会使化学平衡向着气体体积缩小的方向移动;减小压强,会使平衡向着气体体积增大的方向移动。(1分)(只答一方面也给1分)? |
【解析】
试题分析:(1)从右图装置可以看出,该装置利用铜丝和稀硝酸接触反应制备NO,所以发生的反应方程式为:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。
(2)NO与空气混合变红是由于NO被O2氧化生成了红棕色的NO2,所以体现了NO较强的还原性。
(3)该装置是一个制备NO气体的实验装置,制备气体的装置都要检查装置的气密性,所以在所给出的步骤中漏了检查气密性的步骤。该装置用注射器抽走U形管左侧液面上方的空气后压强减小,所以液体硝酸会充满左端并与金属Cu接触发生反应,所以发生反应后观察到的实验现象是U型管短管中溶液与铜丝接触反应,有气泡产生,溶液变蓝色,铜丝溶解减少;由于有气体产生左边液面下降,右边液面上升。
(4)在铜丝上绑上石墨,石墨并不参与反应,但是石墨可以和铜丝构成原电池,石墨作正极,所以可以加快反应制备NO气体。
(5)本题要注意的是题目要求实验探究的目的是外界因素对化学平衡移动影响,所以实验中应该在其他条件不变的情况下,改变某一条件,从而观察现象,由现象得出该反应的实验结论。给出的已知反应方程式能提供的信息是反应有气体参加且正反应是放热反应,NO2有颜色,而N2O4 无色。所以能够控制的使该反应平衡发生改变的条件可以是压强(容器体积)和温度。由于注射器做容器已经在步骤①固定,所以还需要实验的步骤就是改变条件了,要利用好教材中出现的该实验,同时也不要受教材中出现的实验影响而去改变容器,所以合理的实验如下表:方案一:?
实验步骤? | 实验现象? | 实验结论? |
②将二支注射器分别插入装有热水、冰水的烧杯中(1分);几分钟后拿出作对比。(1分)? | 浸入热水的注射器中的气体颜色变深;(1分)? 浸入冰水的注射器中的气体颜色变浅。(1分)? | 在其他条件不变的情况下(1分),温度升高,会使化学平衡向着吸热反应的方向移动;温度降低会使化学平衡向放热反应的方向移动(1分)(只答一方面也给1分)? |
或:方案二:?
实验步骤? | 实验现象? | 实验结论? |
②将一支注射器的活塞迅速往里推到一定位置,然后与另一支注射器的气体作对比(1分);回复原状后再将注射器的活塞迅速往外拉到一定位置,然后与另一支注射器的气体作对比(1分)? | 迅速推动注射器,针管内气体颜色先变深后慢慢变浅(1分);迅速拉伸注射器时,针管内气体颜色先变浅后深慢慢变深。(1分)? | 在其他条件不变的情况下(1分),增大压强,会使化学平衡向着气体体积缩小的方向移动;减小压强,会使平衡向着气体体积增大的方向移动。(1分)(只答一方面也给1分)? |
考点:本题考查的是比较基础的实验探究题,该实验题衔接教材注重细节的考查。


 步步高达标卷系列答案
步步高达标卷系列答案科目:高中化学 来源: 题型:阅读理解
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
 某同学设计如图装置,研究非金属元素性质变化规律.
某同学设计如图装置,研究非金属元素性质变化规律.查看答案和解析>>
科目:高中化学 来源:2013届辽宁省东北育才学校高三第一次模拟考试化学试卷(带解析) 题型:实验题
某同学设计如图装置,研究非金属元素性质变化规律。
(1)已知硅酸(H2SiO3)是一种难溶于水的弱酸,呈白色。在化学反应中,一般地,强酸能制弱酸,如NaHCO3+HCl===NaCl+CO2↑+H2O,得出:HCl酸性强于H2CO3的酸性。现有硝酸溶液、碳酸钙、澄清石灰水、硅酸钠溶液,选择试剂用如图装置证明:酸性:HNO3>H2CO3>H2SiO3。
A中装试剂________,B中装试剂____________,C中装试剂____________。C中实验现象为____________;写出C中发生反应的离子方程式_________________________________________。
(2)已知高锰酸钾在常温下与浓盐酸反应产生氯气,利用如图装置证明氯气氧化性强于碘单质的氧化性。则A中装浓盐酸,B中装入高锰酸钾粉末,C中装试剂________,C中现象________,写出离子方程式__________________。该实验装置有明显不足,请指出改进方法:_______________________________________。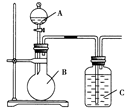
(3)如果C中装饱和的氢硫酸溶液,A中装浓盐酸,B中装高锰酸钾溶液,反应开始后观察到现象是C中产生淡黄色沉淀,写出化学方程式______________________________;
证明氯的非金属性比硫的非金属性________(填“强”或“弱”或“无法判断”)。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年河南省郑州市高三上学期期中考试化学试卷 题型:实验题
(14分)某同学设计如图装置,研究非金属元素性质变化规律。

(1)已知硅酸(H2SiO3)是一种难溶于水的弱酸,呈白色。在化学反应中,一般地,强酸能制弱酸,现有硝酸溶液、碳酸钙、澄清石灰水、硅酸钠溶液,选择试剂用如图装置证明:酸性:HNO3>H2CO3>H2SiO3。
A中装试剂________,B中装试剂________,C中装试剂________。C中实验现象为__________;写出C中发生反应的离子方程式______________________________________。
(2)已知高锰酸钾在常温下与浓盐酸反应产生氯气,利用如图装置证明氯气氧化性强于碘单质的氧化性。则A中装浓盐酸,B中装入高锰酸钾粉末,C中装试剂________,C中现象______________________。写出离子方程式________________________________。该实验该装置有明显不足,请指出改进方法:_____________________________________________。
(3)如果C中装饱和的氢硫酸溶液,A中装浓盐酸,B中装高锰酸钾溶液,反应开始后观察到现象是C中产生淡黄色沉淀,写出化学方程式________________________________;
证明氯的非金属性比硫的非金属性________(填“强”“弱”或“无法判断”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com