
| A、NaHCO3和Al2(SO4)3 |
| B、NaHCO3和Na2CO3 |
| C、MgSO4和CaCO3 |
| D、Na2CO3和Al(NO3)3 |


科目:高中化学 来源: 题型:
 I.已知中和热是指酸跟碱发生中和反应生成lmol H2O时的反应热.
I.已知中和热是指酸跟碱发生中和反应生成lmol H2O时的反应热.| 实验起始温度(℃) | 实验中止温度(℃) | |
| 实验① | 25.00 | 28.64 |
| 实验② | 25.00 | 28.52 |
| 实验③ | 25.00 | 29.66 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、等体积、等物质的量浓度的Ca(HCO3)2溶液和NaOH溶液混合:Ca2++2HCO
| ||||
| B、向明矾溶液中滴加氢氧化钡溶液至SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O | ||||
| C、1molCl2通入含1mol FeI2的溶液中:2Fe2++2I-+2Cl2=2Fe3++4Cl-+I2 | ||||
| D、酸性条件下KIO3溶液与KI溶液发生反应生成I2:IO3-+5I-+3H2O=3I2+6OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
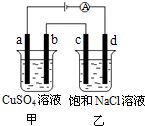 如图,a、b、c、d均为石墨电极,通电进行电解.下列说法正确的是( )
如图,a、b、c、d均为石墨电极,通电进行电解.下列说法正确的是( )| A、乙烧杯中d的电极反应为 2Cl--2e-═Cl2↑ |
| B、a、c两极产生气体的物质的量相等 |
| C、甲、乙两烧杯中溶液的pH均保持不变 |
| D、乙烧杯中通入适量HCl气体,溶液组成可以恢复 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na、Fe分别与不足量的稀硫酸反应所得溶液均呈中性 |
| B、7.8gNa2O2与CO2完全反应,转移0.1 mol电子 |
| C、合金中至少含有两种金属元素 |
| D、NaHCO3、CaCO3、(NH4)2CO3三种固体受热后均能生成气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2O、MgO、Al2O3均属于碱性氧化物 |
| B、石灰石、生石灰、熟石灰均属于碱 |
| C、根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体 |
| D、根据电解质在水溶液中电离的程度,将电解质分为强电解质和弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
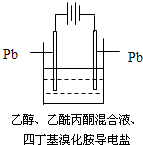 有机电解制备的金属醇盐,可直接作为制备纳米材料的前体.以下是一种电化学合成金属醇盐的主要装置.在电解过程中,已知乙醇和乙酰丙酮(CH3COCH2COCH3)在阴极发生的电极反应为:
有机电解制备的金属醇盐,可直接作为制备纳米材料的前体.以下是一种电化学合成金属醇盐的主要装置.在电解过程中,已知乙醇和乙酰丙酮(CH3COCH2COCH3)在阴极发生的电极反应为:| A、阳极Pb失去电子,发生还原反应 |
| B、当阳极失去2 mol e-时,阴极产生2 mol氢气 |
| C、电解过程中,阳离子向阴极移动 |
| D、已知Pb-4e-=Pb4+,当消耗Pb的质量为103.5 g时,则转移电子2 mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com