
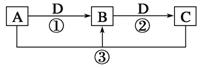
已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同一种元素。在一定条件下它们之间的相互转化关系如图所示(部分反应中的H2O已略去)。
请回答下列问题:
(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,加热蒸干B的溶液不能得到B,则B的化学式可能是__________;工业上制取A的离子方程式_________________________。
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,遇空气会变色,则反应①的化学方程式为____________________________________。
(3)若D是氯碱工业的主要产品之一,B有两性,则反应②的离子方程式是________________________________________________________________。
(4)若A、C、D都是常见气体,C是导致酸雨的主要气体,则反应③的化学方程式为_________________________________________________________。
某同学将搜集到的一定量的酸雨保存在密闭容器中,每隔一定时间测酸雨的pH,发现在起始一段时间内,酸雨的pH呈减小趋势,用离子方程式解释原因: _____________________________________________________________。
 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:
以石墨做电极,电解1 mol/L下列物质的水溶液,下列表述正确的是
A.若为盐酸溶液,pH减小 B.若为氢氧化钠溶液,pH减小
C.若为硫酸钠溶液,pH不变 D.若为氯化钠溶液,pH不变
查看答案和解析>>
科目:高中化学 来源: 题型:
某混合物的水溶液,可能含有以下离子中的若干种:K+、Al3+、Fe3+、Mg2+、Ba2+、NH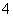 、Cl-、CO
、Cl-、CO 、SO
、SO ,现分别取100 mL的两等份溶液进行如下实验:
,现分别取100 mL的两等份溶液进行如下实验:
①第一份加过量NaOH溶液后加热,收集到0.02 mol气体,无沉淀生成,同时得到溶液甲。
②向甲溶液中通入过量CO2生成白色沉淀,沉淀经过滤、洗涤、干燥、灼烧后,得到1.02 g固体。
③第二份加足量BaCl2溶液后,生成白色沉淀,沉淀经足量盐酸洗涤、干燥后,得到11.65 g固体。
依据实验回答下列问题:
(1)综合以上实验,该混合物的水溶液中一定不存在的离子是 (填离子符号)。
(2)写出②中产生沉淀的离子方程式 。
(3)某同学通过分析认为该溶液中K+一定 (填“存在”或“不存在”),他的理由是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
利用生活中常见的材料可以进行很多科学实验,下图就是一个用废旧材料制作的可用于驱动玩具的电池示意图。当电池工作时,有关说法正确的是( )
A.铝罐将逐渐被腐蚀
B.该电池驱动电动玩具时,石墨棒应与玩具电机的负极相连
C.石墨棒上发生的反应为:O2-4e-+2H2O== 4OH-
D.该电池工作一段时间后石墨棒的质量会减轻

查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E 为五种常见的短周期元素,常温下 A、B 可形成 B2A2 和 B2A 两种液态化合物,B 与 D 可形成分子 X,也可形成阳离子 Y,X、Y 在水溶液中酸、碱性恰好相反,C 元素的焰色反应呈黄色,E 与 C 同周期,且 E 的阳离子在其所在周期元素形成的简单离子中半径最小,试回答:
(1)D元素处于周期表的位置____________。
(2)B2A2 对应化合物的结构式为__________,Y 的电子式为____________。
(3)液态 X 类似 B2A,也能微弱电离且产生电子数相同的两种离子,则液态 X 的电离方程式为______________。
(4)A、D、E 三种元素形成的盐(化学式为 A9D3E)的水溶液呈________性,用离子方程式解释其原因________。
(5)W、Q是由 A、B、C、D 四种元素中任意三种组成的不同类型的强电解质,W的水溶液呈碱性,Q的水溶液呈酸性,且物质的量浓度相同的W、Q溶液中水的电离程度前者小于后者,则W为________,Q为________(填化学式)。
(6)用A单质和B单质可制取气体燃料电池,该电池用多孔的惰性电极浸入浓KOH溶液,两极分别通入A单质和B单质。写出该电池的电极反应方程式:
负极:_______;正极: ________。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有短周期元素构成的3种单质甲、乙、丙,它们在一定条件下能发生如下变化,部分产物已略去。
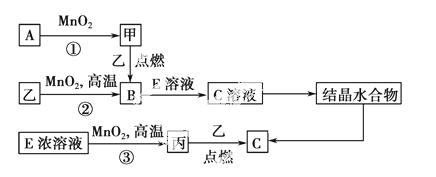
(1)若反应①可在常温下进行,则A的电子式为________。若反应①需在加热条件下进行,则反应①的化学方程式为____________________________。
(2)反应②的化学方程式为________,该反应是________(填“放热”或“吸热”)反应。
(3)从C溶液中得到C需经过两步操作:先从C溶液中得到晶体,再将得到的晶体转化为C。从C溶液中得到晶体的过程被称为________,将得到的晶体转化为C的实验条件是____________________________________。
(4)反应③中氧化剂与还原剂的物质的量之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如图转化关系, 请完成下列问题:
请完成下列问题:
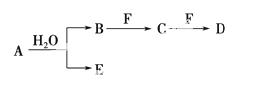
(1)若常温下A为有色气体。
①当F是一种金属单质时,请写出一定浓度的B溶液和适量F反应生成C与气体E的离子方程式:____________________________________________________________________。
②当C为直线形分子时,E具有漂白性,物质F焰色反应呈黄色,则C的电子式为________;D中所含化学键的类型为_________________________________________________________。
(2)若A为淡黄色固体,D为白色难溶于水的物质,且A和D的相对分子质量相等,请用离子方程式表示F的水溶液呈酸性的原因:______________
________________________________________________________________。
(3)若A中一种元素原子的最外层电子数为内层电子总数的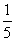 ,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液,请写出A与H2O反应的化学方程式:___________________________________________________________________;
,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液,请写出A与H2O反应的化学方程式:___________________________________________________________________;
B转化为C的化学方程式为____________ ______________________________________________。
______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
种相邻主族短周期元素的相对位置如表,元素X的原子核外电子数是M的2倍,Y的氧化物具有两性。回答下列问题:
| M | N | ||
| X | Y |
(1)元素X在周期表中的位置是第________周期、第________族,其单质可采用电解熔融________的方法制备。
(2)M、N、Y三种元素最高价氧化物对应的水化物中,酸性最强的是________,碱性最强的是________。(填化学式)
(3)气体分子(MN)2的电子式为________。(MN)2称为拟卤素,性质与卤素类似,其与氢氧化钠溶液反应的化学方程式为____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有雨水样品1份,每隔一段时间测定该雨水样品的pH,所得数据如下表:
| 测试时间/h | 0 | 1 | 2 | 3 | 4 |
| 雨水的pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
分析数据,回答下列问题:
(1)雨水样品的pH变化的原因是(用化学方程式表示):
________________________________________________________________________。
(2)如果将刚取样的上述雨水和自来水相混合,pH将变________,原因是(用化学方程式表示):________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com