
| A. | 加入水时,溶液中离子浓度都减小 | |
| B. | 加入少量NaOH固体,平衡向正反应方向移动 | |
| C. | 加入少量0.1mol•L-1CH3COOH溶液,溶液中c(H+)减小 | |
| D. | 加入少量CH3COONa固体,电离平衡常数减小 |
分析 因加入水、加热促进弱电解质的电离,加酸抑制弱酸的电离,加入与弱电解质电离出相同离子的电解质抑制电离,以此来解答.
解答 解:A.加水促进弱电解质的电离,则电离平衡正向移动,平衡状态下离子浓度减小,氢离子浓度减小溶液中氢氧根离子浓度增大,故A错误;
B.加入少量NaOH固体,与CH3COOH电离生成的H+结合,使电离平衡正向移动,故B正确;
C.加入少量0.1mol•L-1CH3COOH溶液,c(H+)增大,故C错误;
D.加入少量CH3COONa固体,由电离平衡可知,c(CH3COO-)增大,则电离平衡逆向移动,温度不变电离平衡常数不变,故D错误;
故选B.
点评 本题考查电离平衡的移动,明确影响平衡移动的因素即可解答,注意利用加水促进电离及同离子效应来分析解答.


科目:高中化学 来源: 题型:选择题
 ”,该物质的一个分子中含有300~500个碳原子,性质很活泼.下列关于该链式炔碳的熔点判断正确的是( )
”,该物质的一个分子中含有300~500个碳原子,性质很活泼.下列关于该链式炔碳的熔点判断正确的是( )| A. | 比石墨高 | B. | 比石墨低 | ||
| C. | 低于石墨而高于金刚石 | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 冰的晶体中每个水分子可与周围两个水分子形成氢键 | |
| B. | 手性碳原子不一定是饱和碳原子 | |
| C. | 区分晶体与非晶体最科学的方法是X-射线衍射法 | |
| D. | 晶体中有阳离子就一定有阴离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实现化石燃料清洁利用,就无需开发新能源 | |
| B. | 垃圾是放错地方的资源,应分类回收利用 | |
| C. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| D. | 为提高农作物的产量和质量,应大量使用化肥和农药 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H5OH | B. | CH4 | C. | C2H4O | D. | C3H8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在排放海水的钢铁阀门上用导线连接一块石墨,一同浸入海水中 | |
| B. | 在海轮舷上用铁丝系住锌板浸在海水里 | |
| C. | 将金属制成防腐蚀的合金如不锈钢 | |
| D. | 在地下输油的铸铁管上接直流电源的负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
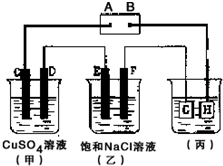 如图所示的装置,C、D、E、F 都是惰性电极.将电源接通后,观察到甲中C电极上有红色固体析出,电解一段时间后,C电极质量增加19.2g,试回答以下问题:
如图所示的装置,C、D、E、F 都是惰性电极.将电源接通后,观察到甲中C电极上有红色固体析出,电解一段时间后,C电极质量增加19.2g,试回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 醋酸溶液能使紫色石蕊溶液变红 | |
| B. | 醋酸溶液能与碳酸钠反应产生二氧化碳气体 | |
| C. | 煮沸醋酸溶液再冷却到常温,发现溶液pH变大 | |
| D. | 浓度均为1mol/L的盐酸和醋酸,前者导电能力强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com