
| A. | 改变某一条件,使v(正)、v(逆)均改变,化学平衡一定移动 | |
| B. | 改变某一条件,使v′(正)>v′(逆)不变,化学平衡一定逆向移动 | |
| C. | 改变某一条件,使v′(正)增大,v′(逆)不变,化学平衡一定正向移动 | |
| D. | 改变某一条件后,v′(正)、v′(逆)同时增大或同时减小时,化学平衡不移动 |
分析 A.改变条件时,正逆反应速率改变且相等时平衡不移动;
B.改变条件时,如果使v′(正)>v′(逆)不变,则平衡正向移动;
C.改变条件时,使v′(正)增大,v′(逆)不变,则v′(正)>v′(逆),平衡正向移动;
D.改变条件时,v′(正)、v′(逆)同时增大或同时减小时,但二者不相等,平衡移动.
解答 解:A.改变条件时,正逆反应速率改变且相等时平衡不移动,如加入催化剂时同等程度的增大正逆反应速率,平衡不移动,故A错误;
B.改变条件时,如果使v′(正)>v′(逆)不变,则平衡正向移动,故B错误;
C.改变条件时,使v′(正)增大,v′(逆)不变,导致v′(正)>v′(逆),正反应速率大于逆反应速率而使平衡正向移动,故C正确;
D.改变条件时,v′(正)、v′(逆)同时增大或同时减小时,但二者不相等,平衡移动,如果正逆反应速率相等则平衡不移动,故D错误;
故选C.
点评 本题考查化学反应速率及化学平衡影响因素,为高频考点,改变条件时要根据正逆反应速率是否相等判断平衡是否移动及移动方向,题目难度不大.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 现以A为主要原料合成乙酸乙酯,其合成路线如图所示.
现以A为主要原料合成乙酸乙酯,其合成路线如图所示.
 A结构式CH2=CH2
A结构式CH2=CH2查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 0.1mol•L-1氨水中,c(OH-)=c(NH4+) | |
| B. | 10 mL 0.02mol•L-1HCl溶液与10 mL 0.02mol•L-1Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=12 | |
| C. | 在0.1mol•L-1CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+) | |
| D. | 0.1mol•L-1某二元弱酸强碱盐NaHA溶液中,c(Na+)=2c(A2-)+c(HA-)+c(H2A) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述反应的产物Cu2HgI4中,Hg的化合价为+2 | |
| B. | 上述反应中CuI既是氧化剂,又是还原剂 | |
| C. | 上述反应中Hg元素与Cu元素均被氧化 | |
| D. | 上述反应中生成 64gCu时,转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H4、C6H6 | B. | CH4、CH2O | C. | C2H6、CH3CHO | D. | C3H8、CH3CH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 原儿茶醛是制造医药及染料的中间体,可用于制造多种抗菌素和消炎药物.其结构如图:请回答:
原儿茶醛是制造医药及染料的中间体,可用于制造多种抗菌素和消炎药物.其结构如图:请回答: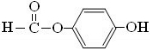 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 根据氧化物的性质将氧化物分成酸性氧化物、碱性氧化物和两性氧化物等 | |
| B. | 根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应 | |
| C. | 根据是否有丁达尔现象将分散系分为溶液、胶体和浊液 | |
| D. | 根据组成元素的种类将纯净物分为单质和化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com